题目内容
9.某学生想在实验室中准确配制2mol/L的NaCl溶液950mL,请回答下列问题:(1)应选用容量瓶的规格1000mL;应称量NaCl固体质量117.0g;
(2)容量瓶上标有以下6项中的哪些项A
①温度 ②浓度 ③容量 ④压强 ⑤刻度线 ⑥酸式和碱式
A、①③⑤B、③⑤⑥C、①②④D、②④⑥
(3)配制时,其正确的操作顺序是(用字母表示,每个字母只用一次)BCAFED
A、用水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
B、用托盘天平准确称取所需的NaCl固体质量,转移至烧杯中,再加入一定量水,用玻璃棒慢慢搅动,使其混合均匀
C.将已溶解完全的NaCl溶液沿玻璃棒注入到的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
(4)配制溶液时,若仪器、药品存在问题,特别是操作不当,都会使所配溶液中溶质的浓度偏高或偏低.试分析下列变化并填写:(填“偏低”、“偏高”或“不变”)
①洗涤液未注入容量瓶中,溶液浓度偏低.
②加水定容超过刻度线,又将多余的水吸出,则溶液中溶质的浓度偏低.
③溶解时未冷却至室温,就转移到容量瓶中,立即定容,则溶液浓度偏高.
④定容时仰视,则所配溶液浓度偏低.
分析 (1)依据配制溶液体积选择容量瓶规格;依据m=CVM计算需要溶质的质量;
(2)依据容量瓶构造解答;
(3)依据配制一定物质的量浓度溶液的一般操作步骤解答;
(4)分析操作对溶质的物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行分析.
解答 解:(1)配制2mol/L的NaCl溶液950mL,应选择1000mL容量瓶,需要溶质的质量m=2mol/L×1L×58.5g/mol=117.0g;
故答案为:1000mL;117.0;
(2)容量瓶上标有:温度、刻度线、容量;
故选:A;
(3)配制一定物质的量浓度溶液的一般操作步骤:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀,所以正确的顺序为:BCAFED;
故答案为:BCAFED;
(4)①洗涤液未注入容量瓶中,导致部分溶质损耗,溶质的物质的量偏小,溶液浓度偏低;
②加水定容超过刻度线,又将多余的水吸出,导致部分溶质损耗,溶质的物质的量偏小,溶液浓度偏低;
③溶解时未冷却至室温,就转移到容量瓶中,立即定容,冷却后,溶液体积偏小,溶液浓度偏高;
④定容时仰视,导致溶液体积偏大,溶液浓度偏低;
故答案为:偏低;偏低;偏高;偏低.
点评 本题考查一定物质的量浓度溶液的配制,明确容量瓶规格选择依据,熟悉依据C=$\frac{n}{V}$进行误差分析的方法是解题关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.下列化学用语表示正确的是( )
| A. | 甲基的电子式: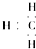 | B. | 乙炔的最简式:C2H2 | ||
| C. | 乙醛的结构简式:CH3COH | D. | 苯分子的比例模型: |
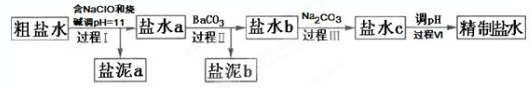
20.氯碱工业电解所用的氯化钠溶液需精制.除去有影响的Ca2+,Mg2+,NH4+,SO42-及泥沙,其精制流程如下:
已知:①Ca2+,Mg2+开始形成相应氢氧化物沉淀的pH如表:
②Ksp(BaSO4)=1.1×10-10,Ksp(BaCO3)=2.6×10-9,Ksp(CaCO3)=5.0×10-9.
下列说法正确的是( )

已知:①Ca2+,Mg2+开始形成相应氢氧化物沉淀的pH如表:
| Ca(OH)2 | Mg(OH)2 | |
| pH | ≥11.5 | ≥4.2 |
下列说法正确的是( )
| A. | 盐泥a除泥沙外,还含有Ca(OH)2和Mg(OH)2 | |
| B. | 过程Ⅰ中NH4+转化为N2的离子方程式是3ClO-+2NH4+═3Cl-+N2↑+3H2O+2H+ | |
| C. | 过程Ⅱ中通入CO2有利于除SO42- | |
| D. | 过程Ⅳ调pH可以使用硝酸 |
17.下列反应的离子方程式正确的是( )
| A. | 将铁粉加入稀硫酸中:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| C. | SiO2与NaOH溶液反应:SiO2+2OH-═SiO32-+H2O | |
| D. | 将氯气通入水中:Cl2+H2O═2H++Cl-+ClO- |
4.下列各组物质的溶液,不用其他试剂就能一一鉴别出来的是( )
| A. | K2SO4、HNO3、BaCl2 | B. | NaOH、NaCl、CuCl2 | ||
| C. | BaCl2、Na2CO3、HCl | D. | KCl、H2SO4、AgNO3 |
1.下列说法正确的是( )
| A. | 按系统命名法,CH3CH(C2H5)CH(C2H5)CH3的名称是2,3-二乙基丁烷 | |
| B. | 等质量的甲醛与乳酸[CH3CH(OH)COOH]完全燃烧消耗氧气的量不相等 | |
| C. | 通过石油裂解可以得到乙烯、丙烯、甲烷、苯、甲苯等重要化工基本原料 | |
| D. | 用Na2CO3溶液能区分CH3COOH、CH3CH2OH、苯、硝基苯四种物质 |
19.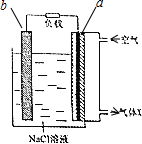 镁-空气电池的工作原理如图所示.下列说法不正确的是( )
镁-空气电池的工作原理如图所示.下列说法不正确的是( )
 镁-空气电池的工作原理如图所示.下列说法不正确的是( )
镁-空气电池的工作原理如图所示.下列说法不正确的是( )| A. | 工作一段时间后,c(Na+)变大 | B. | 气体X中N2的百分量与空气相同 | ||
| C. | 电池工作时,OH-向a极移动 | D. | 电池总反应为2Mg+O2+2H2O═2Mg(OH)2 |