题目内容
下列反应符合如图p-υ变化曲线的是( )


| A、H2(g)+I2(g)?2HI(g) |
| B、3NO2(g)+H2O(l)?2HNO3(l)+NO(g) |
| C、4NH3(g)+5O2(g)?4NO(g)+6H2O(g) |
| D、CO2(g)+C(s)?2CO(g) |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:图象分析可知,平衡后增大压强平衡正向进行,正反应速率大于逆反应速率,据此分析判断;
解答:
解:A、H2(g)+I2(g)?2HI(g),反应是气体体积不变的反应,增大压强平衡不变,u符合图象变化,故A错误;
B、3NO2(g)+H2O(l)?2HNO3(l)+NO(g),反应前后气体体积减小的反应,增大压强平衡正向进行,符合图象变化,故B正确;
C、3NO2(g)+H2O(l)?2HNO3(l)+NO(g),反应前后气体体积增大的反应,增大压强,平衡逆向进行,不符合图象变化,故C错误;
D、CO2(g)+C(s)?2CO(g),反应前后气体体积增大,增大压强平衡逆向进行,图象不符合变化,故D错误;
故选B.
B、3NO2(g)+H2O(l)?2HNO3(l)+NO(g),反应前后气体体积减小的反应,增大压强平衡正向进行,符合图象变化,故B正确;
C、3NO2(g)+H2O(l)?2HNO3(l)+NO(g),反应前后气体体积增大的反应,增大压强,平衡逆向进行,不符合图象变化,故C错误;
D、CO2(g)+C(s)?2CO(g),反应前后气体体积增大,增大压强平衡逆向进行,图象不符合变化,故D错误;
故选B.
点评:本题考查了化学图象分析,平衡移动原理的分析判断,掌握反应特征和平衡移动原理是解题关键,题目较简单.

练习册系列答案
 巧学巧练系列答案
巧学巧练系列答案
相关题目
已知15g化合物A完全氧化,把产物通过浓硫酸和碱石灰,浓硫酸增重9g,碱石灰增重39.6g,用现代物理方法测定:①该有机物的质谱图如图所示 ②核磁共振仪1,3,5测出A的核磁共振氢谱有5个峰,其面积之比为1:2:2:2:3.

则下列说法正确的是( )

则下列说法正确的是( )
| A、该有机物的分子式为C9H10O |
| B、该有机物的摩尔质量为150 |
C、该物质的结构简式可能为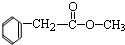 |
| D、该有机物一定不能与Na2CO3反应 |
某学生用NaHCO3和KHCO3组成的某混合物进行实验,测得如下数据(盐酸的物质的量浓度相等),下列分析推理正确的是( )
| 50mL盐酸 | 50mL盐酸 | 50mL盐酸 | |
| m(混合物) | 9.2g | 15.7g | 27.6g |
| VCO2(标况) | 2.24L | 3.36L | 3.36L |
| A、盐酸的物质的量浓度为3.0mol/L |
| B、根据表中数据不能计算出混合物中NaHCO3的质量分数 |
| C、向50mL盐酸中加入混合物27.6g时,盐酸过量 |
| D、15.7g混合物能恰好与盐酸完全反应 |
锂电池是新型高能电池,它以质轻、容量大而受到重视.目前已经制成多种功能的锂电池.某种锂电池的总反应可表示为:Li+MnO2→LiMnO2.若该电池提供0.5C电量,则消耗正极材料的质量约为(其他损耗忽略不计)( )
| A、3.5g |
| B、7g |
| C、4.52×10-4g |
| D、43.5g |
物质的量相同的镁和铝,跟足量的盐酸反应,失去电子数之比为( )
| A、1:1 | B、2:3 |
| C、24:27 | D、3:4 |
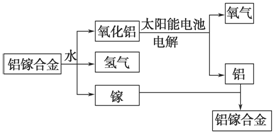 美国普度大学研究开发出一种利用铝镓合金制备氢气的新工艺(如图所示).下列有关该工艺的说法错误的是( )
美国普度大学研究开发出一种利用铝镓合金制备氢气的新工艺(如图所示).下列有关该工艺的说法错误的是( )| A、该过程中,能量的转化形式只有两种 | ||||
| B、铝镓合金可以循环使用 | ||||
C、铝镓合金与水反应的化学方程式为:2Al+3H2O
| ||||
D、总反应式为2H2O
|
下列有关基本营养物质的说法中,正确的是( )
| A、淀粉遇碘化钾溶液变蓝 |
| B、糖类、油脂、蛋白质都是由C、H、O三种元素组成 |
| C、蔗糖和麦芽糖互为同分异构体 |
| D、纤维素在人体内最终水解为葡萄糖 |
下列比较正确的是( )
| A、原子序数:F>Na |
| B、原子半径:r(Na)>r(Al) |
| C、金属性:Al>Mg |
| D、氢化物稳定性:H2S>HCl |