题目内容
为探究亚硫酸钠的热稳定性,某探究性学习小组将无水亚硫酸钠隔绝空气加热,并利用受热后的固体试样和下图的实验装置进行实验,请回答下列问题:
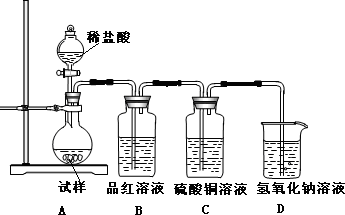
(1)装置A中盛装稀盐酸的仪器名称是 ,装置B的作用是 ;
(2)查阅资料:无水亚硫酸钠隔绝空气受热到600℃才开始分解,且分解产物只有硫化钠和另外一种固体,则SO3 固体加热到600℃以上分解的化学方程式为 ;如果加热温度低于600℃,向所得固体试样中缓缓滴加稀盐酸至足量,在滴加稀盐酸的整个过程中HSO3- 的物质的量浓度变化趋势为 ;
(3)如果加热温度高于600℃,一段时间后,向所得固体试样中缓缓滴加稀盐酸至足量,观察到烧瓶中出现淡黄色沉淀,且有大量气泡产生,则固体试样跟盐酸反应生成淡黄色沉淀的离子方程式为 ,此时B、C装置可能观察到的现象为 .

(1)装置A中盛装稀盐酸的仪器名称是
(2)查阅资料:无水亚硫酸钠隔绝空气受热到600℃才开始分解,且分解产物只有硫化钠和另外一种固体,则SO3 固体加热到600℃以上分解的化学方程式为
(3)如果加热温度高于600℃,一段时间后,向所得固体试样中缓缓滴加稀盐酸至足量,观察到烧瓶中出现淡黄色沉淀,且有大量气泡产生,则固体试样跟盐酸反应生成淡黄色沉淀的离子方程式为
考点:性质实验方案的设计
专题:实验设计题
分析:(1)根据仪器的特点以及二氧化硫的性质来回答;
(2)Na2SO3固体加热到600℃以上分解生成硫化钠和硫酸钠;由题意,Na2SO3要加热到600度以上才分解,因此题中加热温度600度以下冷却后得到的固体仍为Na2SO3;
(3)加热温度为700℃,向所得固体试样中缓缓滴加稀盐酸至足量,观察到烧瓶中出现淡黄色沉淀,且有大量气泡产生,说明加热分解后的固体中含硫化钠和为分解的亚硫酸钠.
(2)Na2SO3固体加热到600℃以上分解生成硫化钠和硫酸钠;由题意,Na2SO3要加热到600度以上才分解,因此题中加热温度600度以下冷却后得到的固体仍为Na2SO3;
(3)加热温度为700℃,向所得固体试样中缓缓滴加稀盐酸至足量,观察到烧瓶中出现淡黄色沉淀,且有大量气泡产生,说明加热分解后的固体中含硫化钠和为分解的亚硫酸钠.
解答:
解:(1)装置A中盛装稀盐酸的仪器名称是分液漏斗,盐酸可以和亚硫酸钠之间反应生成二氧化硫气体,二氧化硫能使品红褪色,所以品红的作用是检验二氧化硫是否生成的,
故答案为:分液漏斗;检验二氧化硫是否存在;
(2)依据题意判断,亚硫酸钠加热到600℃以上分解生成硫化钠和硫酸钠,反应的化学方程式为4Na2SO3
Na2S+3Na2SO4;由题意,Na2SO3要加热到600度以上才分解,因此题中加热温度600度以下冷却后得到的固体仍为Na2SO3向此固体中滴加HCl后,一方面是Na2SO3固体溶于水,这将导致溶液中SO32-浓度增大;另一方面是HCl与SO32-反应,这将导致SO32-浓度减小生成亚硫酸氢根离子浓度增大;加入HCl到一定程度时,SO32-已完全转化为HSO3-,此时前者作用消失,完全是后者起作用,HSO3-浓度先增大后将逐渐减小,直至最后下降到接近于零,
故答案为:4Na2SO3
Na2S+3Na2SO4;先逐渐增大,后逐渐减小;
(3)如果加热温度为700℃,向所得固体试样中缓缓滴加稀盐酸至足量,观察到烧瓶中出现淡黄色沉淀为硫,且有大量气泡产生说明为二氧化硫,则固体试样跟盐酸反应生成淡黄色沉淀的离子方程式为:2S2-+SO32-+6H+=3S↓+3H2O;生成二氧化硫的反应为SO32-+2H+=SO2↑+H2O,此时在B、C两装置中可能观察到得现象为二氧化硫具有漂白作用使品红褪色,生成的气体不是硫化氢通过硫酸铜无现象,B中无明显变化,C中产生黑色沉淀,
故答案为:2S2-+SO32-+6H+=3S↓+3H2O;B中品红溶液褪色,C中无明显变化或B中无明显变化,C中产生黑色沉淀.
故答案为:分液漏斗;检验二氧化硫是否存在;
(2)依据题意判断,亚硫酸钠加热到600℃以上分解生成硫化钠和硫酸钠,反应的化学方程式为4Na2SO3
| ||
故答案为:4Na2SO3
| ||
(3)如果加热温度为700℃,向所得固体试样中缓缓滴加稀盐酸至足量,观察到烧瓶中出现淡黄色沉淀为硫,且有大量气泡产生说明为二氧化硫,则固体试样跟盐酸反应生成淡黄色沉淀的离子方程式为:2S2-+SO32-+6H+=3S↓+3H2O;生成二氧化硫的反应为SO32-+2H+=SO2↑+H2O,此时在B、C两装置中可能观察到得现象为二氧化硫具有漂白作用使品红褪色,生成的气体不是硫化氢通过硫酸铜无现象,B中无明显变化,C中产生黑色沉淀,
故答案为:2S2-+SO32-+6H+=3S↓+3H2O;B中品红溶液褪色,C中无明显变化或B中无明显变化,C中产生黑色沉淀.
点评:本题考查了物质性质验证的实验设计和实验分析判断,主要考查硫及其化合物性质的应用,题目难度中等.

练习册系列答案
相关题目
下列物质的性质与氢键无关的是( )
| A、冰的密度比液态水的密度小 |
| B、NH3易液化 |
| C、H2Se沸点比H2S的沸点高 |
| D、NH3极易溶于水 |
常温下,下列分子或离子在指定的分散系中可以大量共存的一组是( )
A、在pH=1的溶液中,能大量共存的一组离子或者分子:K+、Cr2O
| ||||
| B、c(H+)=10-12mol/L的溶液:Na+、Ba2+、Cl-、Br- | ||||
C、由水电离出的c(H+)=10-14mol/L的溶液:Ca2+、K+、Cl-、HCO
| ||||
| D、0.1mol/L的NaAlO2溶液中:Al3+、Na+、Cl-、SO42- |





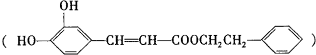 ,在一定条件下能发生如图所示的转化:
,在一定条件下能发生如图所示的转化: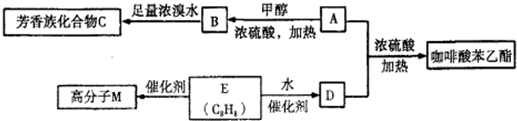
 二茂铁(如图)是一种有机过渡金属化合物,不溶于水,易溶于苯、乙醚等有机溶剂.由烃A可制备二茂铁.A分子是一种没有侧链的环状结构,其一氯取代物有三种,1molA最多可与2molBr2加成,其与Br2的1:1加成只得两种产物.
二茂铁(如图)是一种有机过渡金属化合物,不溶于水,易溶于苯、乙醚等有机溶剂.由烃A可制备二茂铁.A分子是一种没有侧链的环状结构,其一氯取代物有三种,1molA最多可与2molBr2加成,其与Br2的1:1加成只得两种产物.