题目内容
7.氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一种反应物”在40℃~50℃时反应可生成它.CuH不稳定、易分解,CuH在氯气中能燃烧,跟盐酸反应能产生气体,以下有关它的推断中错误的是( )| A. | “另一种反应物”一定具有还原性 | B. | “另一种反应物”一定只具有氧化性 | ||
| C. | 2CuH+3Cl2 $\frac{\underline{\;点燃\;}}{\;}$2CuCl2+2HCl | D. | CuH既可作氧化剂也可作还原剂 |
分析 A.Cu元素的化合价由+2价降低为+1价,在反应中CuSO4作氧化剂;
B.氧化还原反应中,氧化剂具有氧化性,还原剂具有还原性;
C.CuH跟氯气反应生成CuCl2和HCl;
D.氧化还原反应中,既能升高又能降低,既可作氧化剂也可作还原剂.
解答 解:A.Cu元素的化合价由+2价降低为+1价,在反应中CuSO4作氧化剂,则“另一种反应物”在反应中作还原剂,一定具有还原性,故A正确;
B.Cu元素的化合价由+2价降低为+1价,在反应中CuSO4作氧化剂,则“另一种反应物”在反应中作还原剂,具有还原性,故B错误;
C.CuH跟氯气反应生成CuCl2和HCl,则点燃时的方程式为:2CuH+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2CuCl2+2HCl,故C正确;
D.CuH中Cu元素为+1价,既能升高又能降低,所以CuH既可做氧化剂也可做还原剂,故D正确;
故选B.
点评 本题考查氧化还原反应,注意利用信息及反应中元素的化合价变化来解答,题目难度不大,注重知识的迁移应用.

练习册系列答案
 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
相关题目
18.a、b、c、d为短周期元素,a的M电子层有1个电子,b的最外层电子数为内层电子数的2倍,c的最高化合价为最低化合价绝对值的3倍,c与d同周期,d的原子半径小于c.下列叙述错误的是( )
| A. | d元素的非金属性最强 | |
| B. | 它们均存在两种或两种以上的氧化物 | |
| C. | a可与c、d元素分别形成离子化合物 | |
| D. | b、c、d在化学反应中均易得到电子 |
2.下列关于元素周期表的说法正确的是( )
| A. | 单质能与水反应生成强碱的金属元素都在ⅠA族 | |
| B. | L层上的电子数为奇数的元素一定是主族元素 | |
| C. | 稀有气体元素原子的最外层电子数均为8 | |
| D. | 元素周期表有18个纵行,分列16个族,即7个主族、8个副族和一个零族 |
12.下列元素中,原子半径最大的是( )
| A. | 锂 | B. | 钠 | C. | 氟 | D. | 氯 |
19.下列物质中,不能用作漂白剂的是( )
| A. | SO2 | B. | Ca(ClO)2 | C. | NaClO | D. | HCl |
16.下列叙述能证明金属A的金属性比金属B强的是( )
| A. | A原子的最外层电子数比B原子最外层电子数少 | |
| B. | 常温下,A能从冷水中置换出氢气,而B不能 | |
| C. | 等物质的量A和B与足量稀硫酸反应,产生氢气的量A比B多 | |
| D. | A原子的电子层数比B原子电子层数多 |

 ;
;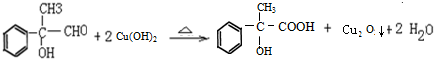 .
.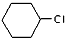 为原料合成重要的化工产品
为原料合成重要的化工产品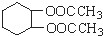 的路线流程图(无机试剂任选)
的路线流程图(无机试剂任选)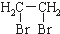
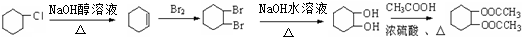 .
. NH4++OH-;实验室制备A的氢化物的化学方程式为Ca(OH)2+2NH4Cl $\frac{\underline{\;\;△\;\;}}{\;}$ CaCl2+2NH3↑+2H2O.
NH4++OH-;实验室制备A的氢化物的化学方程式为Ca(OH)2+2NH4Cl $\frac{\underline{\;\;△\;\;}}{\;}$ CaCl2+2NH3↑+2H2O.