题目内容
4.含1molAlCl3的溶液中加入含3.5molNaOH的溶液,生成沉淀的质量是多少?分析 含1molAlCl3的溶液中加入含3.5molNaOH的溶液,首先发生Al3++3OH-=Al(OH)3↓,然后发生Al(OH)3+OH-=AlO2-+H2O,结合方程式解答该题.
解答 解:含1molAlCl3的溶液中加入含3.5molNaOH的溶液,首先发生Al3++3OH-=Al(OH)3↓,由方程式可知消耗3molNaOH,
然后发生Al(OH)3+OH-=AlO2-+H2O
1 1
0.5mol 3.5mol-3mol,
可知剩余n(Al(OH)3)=1mol-0.5mol=0.5mol,
m(Al(OH)3)=0.5mol×78g/mol=39g,
答:生成沉淀的质量是39g.
点评 本题考查化学方程式的计算,侧重于学生的分析能力和计算能力的考查,为高频考点,注意把握氯化铝与氢氧化钠反应的特征,难度不大.

练习册系列答案
相关题目
1.下列离子方程式书写正确的是( )
| A. | H2SO4与 Ba(OH)2 溶液反应:Ba2++SO42-+H++OH-═BaSO4↓+H2O | |
| B. | 金属钠与水的反应:Na+H2O═Na++OH-+H2↑ | |
| C. | 向足量NaHCO3溶液中滴人少量Ca(OH)2溶液:Ca2++2OH-+2HCO3-═CaCO3↓+2H2O+CO32- | |
| D. | 常温下,将氯气通人水中:Cl2+H2O═2H++2Cl-+ClO- |
19.已知某饱和溶液的①溶液质量,②溶剂质量,③溶液体积,④溶质的摩尔质量,⑤溶质的溶解度,⑥溶液的密度.利用以上部分已知条件不能计算出该饱和溶液的物质的量的浓度的是( )
| A. | ①②④⑥ | B. | ②④⑤ | C. | ①②③④ | D. | ④⑤⑥ |
9.下列说法不正确的是( )
| A. | 在同一条件下不同物质有不同的熵值,其体系的混乱程度越大,熵值越大 | |
| B. | 焓变是一个反应能否自发进行相关的因素,多数放热反应能自发进行 | |
| C. | 一个反应能否自发进行,与焓变和熵变的共同影响有关 | |
| D. | 自发进行的反应一定能迅速进行 |
13.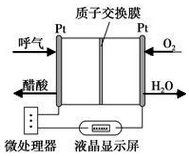 查司机酒驾的一种酸性染料电池酒精检测仪示意如图,它适合现场吹气酒精检测.下列说法不正确的是( )
查司机酒驾的一种酸性染料电池酒精检测仪示意如图,它适合现场吹气酒精检测.下列说法不正确的是( )
 查司机酒驾的一种酸性染料电池酒精检测仪示意如图,它适合现场吹气酒精检测.下列说法不正确的是( )
查司机酒驾的一种酸性染料电池酒精检测仪示意如图,它适合现场吹气酒精检测.下列说法不正确的是( )| A. | 电流由呼气所在的铂电极流出 | |
| B. | O2所在的铂电极处发生还原反应 | |
| C. | 该电池工作一段时间后,正极区pH减小 | |
| D. | 该电池的负极反应式为:CH3CH2OH-4e-+H2O=CH3COOH+4H+ |
14.为提纯下列物质(括号内为杂质),选用的试剂和分离方法都正确的是( )
| 选项 | 物质 | 试剂 | 分离方法 |
| A | 乙酸乙酯(乙酸) | 氢氧化钠溶液 | 分液 |
| B | 苯(苯酚) | 饱和溴水 | 过滤 |
| C | 乙烷(乙烯) | 溴水 | 洗气 |
| D | 乙烯(二氧化硫) | 酸性高锰酸钾溶液 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |

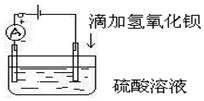 如图所示是某化学兴趣小组探究溶液中离子浓度与溶液导电性的关系.
如图所示是某化学兴趣小组探究溶液中离子浓度与溶液导电性的关系.