题目内容
将1molA(气)和3molB(气)混合后充入2L的密闭容器中,发生如下反应:2A(气)+B(气)?2C(气),10min后反应达到平衡,同温同压下测得反应前后气体的密度之比为9:10.求
(1)A物质的平均反应速率.
(2)A物质的转化率.
(3)反应后气体的压强与反应前压强之比.
(1)A物质的平均反应速率.
(2)A物质的转化率.
(3)反应后气体的压强与反应前压强之比.
考点:化学平衡的计算
专题:化学平衡专题
分析:(1)反应两边都是气体,气体的质量不变,密度与气体的物质的量成反比;根据三段式列式计算出A的平均反应速率;
(2)A转化率=
×100%;
(3)压强之比大于物质的量之比,据此进行计算.
(2)A转化率=
| 消耗量 |
| 起始量 |
(3)压强之比大于物质的量之比,据此进行计算.
解答:
解:(1)设A的转化率为x,气体的密度比与物质的量之比成反比,
对于反应:2A(g)+B(g)?2C(g),
开始(mol):1 3 0
变化(mol):1×x 0.5x x
平衡(mol) 1-x 3-0.5x x
根据密度之比列式为:(1-x+3-0.5x+x):(1+3)=9:10,
解得:x=0.8,即转化率为80%,
10minA消耗了0.8mol,消耗的浓度为:
mol/L=0.4mol/L,
A的平均反应速率为:
=0.04mol/(L?min),
答:A物质的平均反应速率为0.04mol/(L?min);
(2)依据(1)计算可知A的转化率为80%,答:A物质的转化率为80%;
(3)由于压强之比等于物质的量之比,所以反应后气体的压强与反应前压强之比为:
=9:10,
答:反应后气体的压强与反应前压强之比为9:10.
对于反应:2A(g)+B(g)?2C(g),
开始(mol):1 3 0
变化(mol):1×x 0.5x x
平衡(mol) 1-x 3-0.5x x
根据密度之比列式为:(1-x+3-0.5x+x):(1+3)=9:10,
解得:x=0.8,即转化率为80%,
10minA消耗了0.8mol,消耗的浓度为:
| 0.8 |
| 2 |
A的平均反应速率为:
| 0.4mol/L |
| 10min |
答:A物质的平均反应速率为0.04mol/(L?min);
(2)依据(1)计算可知A的转化率为80%,答:A物质的转化率为80%;
(3)由于压强之比等于物质的量之比,所以反应后气体的压强与反应前压强之比为:
| 1-0.8+3-0.4+0.8 |
| 1+3 |
答:反应后气体的压强与反应前压强之比为9:10.
点评:本题考查化学反应速率的有关计算,难度不大,化学反应速率的计算可以用定义法也可以用化学计量数法.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
下列说法正确的是( )
| A、纤维素属于髙分子化合物,与淀粉互为同分异构体,水解后均生成葡萄糖 |
| B、2,3一二甲基丁烷的H一NMR上有5个峰 |
| C、含5个碳原子的有机物,每个分子中最多可形成4个C一C单键 |
D、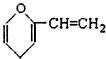 某有机物结构如图所示,该有机物属于芳香族化合物的同分异构体有5种,其中遇FeCl3能显色的有3种 |