题目内容
3.A、B、C、D是中学化学常见单质,其中C、D是常见金属,构成它们的元素的原子序数分别为a、b、c、d,且2(a+b)=3(c-a);X、Y、Z、M、N、W、H、K是常见化合物,M为白色沉淀,它们之间有如图转化关系(图中反应物和生成物中的H2O已略去)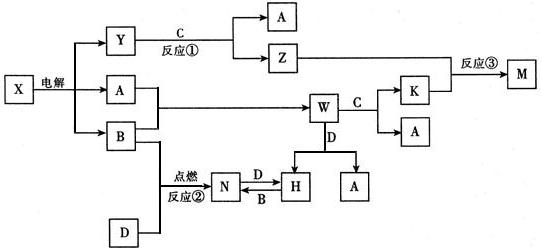
回答下列问题:
(1)写出M的化学式Al(OH)3;
(2)指出元素D在元素周期表中的位置四周期,VIII族;
(3)C、D与Y的浓溶液能形成原电池,写出负极的电极反应式Al+4OH--3e-═AlO2-+2H2O;
(4)写出反应③的离子方程式Al3++3AlO2+6H2O═4Al(OH)3↓;
(5)25时,pH=5的W和N的水溶液中,由水电离出来的c(H+)浓度之比为1:104.
分析 X$\stackrel{电解}{→}$A+B+Y,可以初步推断X为NaCl溶液电解生成了H2、Cl2、NaOH;题中B+D→N以及N与H的相互转化可知金属D为变价金属,应为Fe,则B为Cl2,N为FeCl3,H为FeCl2,由转化关系可知W为HCl,则A为H2,Y为NaOH,金属C可与氢氧化钠溶液反应,应为Al,则Z为NaAlO2,K为AlCl3,M为Al(OH)3,以此解答该题.
解答 解:(1)由以上分析可知M为,故答案为:Al(OH)3;
(2)D为Fe,位于周期表四周期,VIII族,故答案为:四周期,VIII族;
(3)由于铝与氢氧化钠溶液反应,而铁不反应,形成原电池时,铝为负极,被氧化生成AlO2-,电极方程式为Al+4OH--3e-═AlO2-+2H2O,
故答案为:Al+4OH--3e-═AlO2-+2H2O;
(4)转化关系中反应③是Z(NaAl02)+K(AlCl3)→M(Al(OH)3)的离子方程式为:Al3++3AlO2-+6H2O=4Al(OH)3↓,
故答案为:Al3++3AlO2+6H2O═4Al(OH)3↓;
(5)25℃时,PH=5的HCl溶液和FeCl3的水溶液中由H2O电离出来的H+离子浓度之比,依据溶液中存在的离子积常数计算,PH=5的HCl溶液中[H+]酸•[OH-]水=10-14;[H+]水=[OH-]水=10-9mol/L;PH=5的FeCl3的水溶液中存在水解平衡溶液中存在离子积[H+]水•[OH-]剩余=10-14;[H+]水=[OH-]水=10-5;25℃时,PH=5的HCl溶液和FeCl3的水溶液中由H2O电离出来的H+离子浓度之比为10-9:10-5=1:104 故答案为:1:104.
点评 本题考查了元素化合物的物质推断,为高考常见题型,侧重考查学生的分析能力,题目涉及饱和食盐水的电解产物的分析判断,铝及其化合物、铁及其化合物的性质应用,水溶液中的离子积的应用,综合性较强,难度较大.

| A. | 向滴有酚酞的水中加入过量Na2O2粉末并振荡,溶液由无色变红又变无色 | |
| B. | 钠的化学性质非常活泼,钠元素只能以化合态存在于自然界 | |
| C. | 将一小粒金属钠投入水和苯的混合体系中,钠在苯与水的界面处反应并可能作上、下跳动 | |
| D. | 某物质灼烧时,焰色反应为黄色,该物质一定只含钠元素 |
| A. | N2H4的摩尔质量为32 | |
| B. | 1 molN2H4的质量为32 g•mol-1 | |
| C. | 在标准状况下,1 mol N2H4的体积约为22.4L | |
| D. | 6.02×1023个N2H4分子的质量为32g |
| A. | 1:5 | B. | 1:2 | C. | 3:2 | D. | 2:1 |
| A. | 2Fe+3Cl2 $\frac{\underline{\;点燃\;}}{\;}$2FeCl3 | B. | NH4Cl $\frac{\underline{\;\;△\;\;}}{\;}$ NH3↑+HCl↑ | ||
| C. | 2Na+2H2O═2NaOH+H2↑ | D. | Cl2+2KI═2KCl+I2 |
| A. | 0.1 mol•L-1 KSCN溶液中:Fe3+、NH4+、Br-、SO42- | |
| B. | $\frac{{c(O{H^-})}}{{c({H^+})}}$=106的溶液中:NH4+、K+、AlO2-、NO3- | |
| C. | 能使甲基橙变红的溶液中:Cu2+、Mg2+、SO42-、Cl- | |
| D. | 0.1 mol•L-1 Ca(NO3)2溶液中:Na+、NH4+、CO32-、CH3COO- |
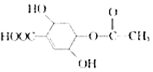 的叙述中不正确的是( )
的叙述中不正确的是( )| A. | 该物质能发生水解反应,1 mol该有机物能与2mo1的NaOH反应 | |
| B. | 该物质可使溴水褪色 | |
| C. | 该物质与Na2CO3溶液反应放出CO2 | |
| D. | 该物质遇FeCl3溶液显色 |
| A. | 碳酸钠固体 | B. | 硝酸钾溶液 | C. | 碳酸钠溶液 | D. | 醋酸钠固体 |