题目内容
18.回答下列问题(1)标况下33.6L CO2的物质的量为1.5mol,质量为66g,所含O原子的数目是1.806×1024个
(2)500ml 1.5mol/L的H2SO4溶液加水稀释成1L溶液后,C(H2SO4)=0.75mol•L-1.
(3)同温同压下,同体积的氨(NH3)和硫化氢(H2S)气体的质量比1:2;同质量的氨和硫化氢气体的体积比是2:1;同质量的氨和硫化氢气体所含氢原子个数之比是3:1.
分析 (1)依据n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$=$\frac{V}{{V}_{m}}$计算;
(2)根据c=$\frac{n}{V}$;
(3)同温同压下,气体摩尔体积相等,相同体积的氨气(NH3)和硫化氢气体(H2S)的物质的量相等,根据m=nM计算其质量之比,根据V=$\frac{m}{M}{V}_{m}$计算相同质量的氨和硫化氢气体的体积之比;根据N=$\frac{m}{M}{N}_{A}$结合分子构成计算其H原子个数之比.
解答 解:(1)标况下33.6L CO2的物质的量为$\frac{33.6L}{22.4L/mol}$=1.5mol; 质量为:1.5mol×44g/mol=66g;所含O原子的数目是1.806×1024,
故答案为:1.5mol; 66g; 1.806×1024;
(2)500ml 1.5mol/L的H2SO4溶液中溶质的物质的物质的量为:0.5L×1.5mol/L=0.75mol,所以c(H2SO4)=0.75mol•L-1,
故答案为:0.75mol•L-1;
(3)同温同压下,气体摩尔体积相等,相同体积的氨气(NH3)和硫化氢气体(H2S)的物质的量相等,根据m=nM知,相同物质的量时其质量之比等于摩尔质量之比=17g/mol:34g/mol=1:2;
根据V=$\frac{m}{M}{V}_{m}$计算相同质量的氨和硫化氢气体的体积之比等于摩尔质量反比=34g/mol:17g/mol=2:1;
根据N=$\frac{m}{M}{N}_{A}$知,相同质量时其分子数之比等于摩尔质量反比=34g/mol:17g/mol=2:1,结合分子构成知,其原子个数之比=(2×3):(1×2)=3:1,
故答案为:1:2;2:1;3:1.
点评 本题考查了物质的量有关计算,明确以物质的量为核心计算公式是解题关键,注意物质的结构组成,注意气体摩尔体积使用条件和对象.

 阅读快车系列答案
阅读快车系列答案| A. | CH3CH2CH2Cl在碱性溶液中水解 | |
| B. | CH2═CH-CH═CH2与H2按物质的量之比为1:1进行反应 | |
| C. | CH3CH═CH2与HCl加成 | |
| D. |  与NaOH的醇溶液共热 与NaOH的醇溶液共热 |
| A. | 已知C(石墨,s)=C(金刚石,s)△H>0 则金刚石比石墨稳定 | |
| B. | 已知2H2(g)+O2(g)=2H2O(l)△H=-571.6 kJ/mol 则H2的燃烧热为285.8 kJ/mol | |
| C. | 已知2C(s)+O2(g)=2CO(g)△H=-221.0 kJ/mol 则C(碳)的燃烧热为110.5 kJ/mol | |
| D. | 已知2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l)△H=-114.6 kJ/mol 则该反应的中和热为114.6 kJ/mol |
| A. | X- | B. | 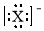 | C. | 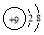 | D. | 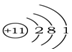 |
 莽草酸是一种合成治疗甲型H1N1流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中,下列关于这两种有机化合物的说法正确的是( )
莽草酸是一种合成治疗甲型H1N1流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中,下列关于这两种有机化合物的说法正确的是( )| A. | 两种酸都能与溴水反应 | |
| B. | 两种酸遇三氯化铁溶液都显色 | |
| C. | 鞣酸分子与莽草酸分子相比多了两个碳碳双键 | |
| D. | 等物质的量的两种酸能消耗等量的NaOH |
| A. | 从海水中可以获得NaCl,NaCl是生产纯碱的原料 | |
| B. | 硅的晶体可以作为光电转换材料用于太阳能电池 | |
| C. | 明矶净水的原理和“84”消毒液的原理相同 | |
| D. | 燃放的焰火是某些金属元素焰色反应所呈现出来的色彩 |
 电浮选凝聚法是工业上的一种污水处理方法,即保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3胶体,Fe(OH)3胶体具有吸附作用,可吸附水中的污物而使其沉淀下来,起到净水的作用,其原理如图所示.下列说法正确( )
电浮选凝聚法是工业上的一种污水处理方法,即保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3胶体,Fe(OH)3胶体具有吸附作用,可吸附水中的污物而使其沉淀下来,起到净水的作用,其原理如图所示.下列说法正确( )| A. | 石墨电极上发生氧化反应 | |
| B. | 甲烷燃料电池中CO32-向空气一极移动 | |
| C. | 根据图示,物质A为CO2 | |
| D. | 为增强污水的导电能力,可向污水中加入适量乙醇 |

| A. | CH3CH2CH3 | B. | CH3CH2CH2OH | C. | (CH3)2CHCH3 | D. | CH3CH2CHO |