题目内容
25℃,101.3KPa时,1g甲醇(CH4O)完全燃烧生成CO2和H2O(l),同时放出22.68KJ热量,试写出这个燃烧反应的热化学方程式 ,甲醇的燃烧是 .
考点:热化学方程式,燃烧热
专题:
分析:燃烧热是1mol可燃物完全燃烧生成稳定氧化物时放出的热量;在25℃、101kPa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ,32g甲醇燃烧生成CO2和液态水时放热22.68kJ×32=725.76kJ,1mol甲醇质量为32克,所以完全燃烧1mol甲醇生成二氧化碳和液态水放热725.76KJ;
解答:
解:1mol甲醇完全燃烧生成二氧化碳和液态水放热725.8KJ;燃烧热的热化学方程式为:CH3OH(l)+
O2(g)═CO2(g)+2H2O(l)△H=-725.76 kJ?mol-1,
故答案为:CH3OH(l)+
O2(g)═CO2(g)+2H2O(l)△H=-725.76 kJ?mol-1;725.76 kJ?mol-1.
| 3 |
| 2 |
故答案为:CH3OH(l)+
| 3 |
| 2 |
点评:本题考查热化学反应方程式的书写与燃烧热的相关知识,题目难度不大.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案
相关题目
下列分离提纯物质的操作中,错误的是( )
| A、用过滤的方法除去食盐中的泥沙 |
| B、用分液的方法分离汽油和水 |
| C、用结晶的方法分离氯化钠和硝酸钾 |
| D、用加热的方法除去碳酸氢钠中混有的碘 |
下列物质中,不属于醇类的是( )
| A、C3H7OH |
| B、C6H5OH |
| C、C6H5CH2OH |
| D、甘油 |
不具备食品防腐作用的物质是( )
| A、醋 | B、糖 | C、食盐 | D、水 |
以下对生活事实的解释,不正确的是( )
| A、食品添加剂虽然能改善食物的色、香、味,但由于他们对健康有害,均不宜食用 |
| B、厨房里洗涤油污,常用碱性洗涤剂,因为植物油会在碱性溶液中水解 |
| C、用灼烧的方法可以区别人造丝和蚕丝,因为蚕丝是蛋白质,灼热时产生具有烧焦羽毛的气味 |
| D、高温消毒是通过加热的方法使细菌的蛋白质变性而死亡 |
下列冶炼金属的化学原理错误的是( )
A、2NaCl(熔融)
| ||||
B、MgO+H2
| ||||
C、2Al2O3(熔融)
| ||||
D、Fe2O3+3CO
|
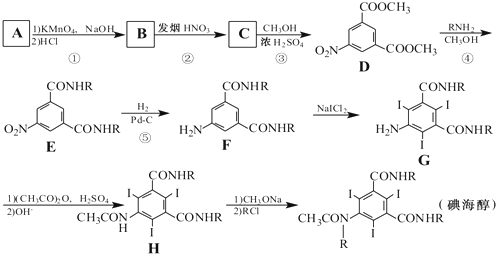
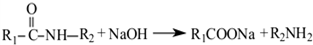
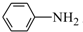 呈弱碱性,易被氧化请写出以和(CH3CO)2O为原料制备染料中间体
呈弱碱性,易被氧化请写出以和(CH3CO)2O为原料制备染料中间体 的合成路线流程图(无机试剂任用)
的合成路线流程图(无机试剂任用)