题目内容
5.根据教材中的“中和热的测定实验”,所用玻璃仪器除了烧杯、量筒、胶头滴管以外,还需要温度计和搅拌器.已知:含有10.0g氢氧化钠的稀溶液与足量的稀盐酸反应,放出14.3kJ的热量,则该中和反应的中和热为57.2KJ.分析 根据中和热的测定实验用到的仪器知识来回答;根据中和热是强酸强碱发生反应生成1mol水放出的热量计算.
解答 解:中和热的测定实验用到的玻璃仪器有:烧杯、温度计、量筒、搅拌器、胶头滴管,则还需要温度计和搅拌器;
中和热是强酸强碱发生反应生成1mol水放出的热量,则含有10.0g氢氧化钠的稀溶液与足量的稀盐酸反应,放出14.3kJ的热量,则该中和反应的中和热为$\frac{14.3}{\frac{10.0}{40}}$=57.2KJ,
故答案为:温度计和搅拌器;57.2KJ.
点评 本题为有关中和热测定的实验以及中和热的计算,较基础,考查学生分析和解决问题的能力,难度不大.

练习册系列答案
相关题目
15.下列物质与水反应会放出氧气的是( )
| A. | Na | B. | SO2 | C. | Na2O2 | D. | NO2 |
16.下列说法,错误的是( )
| A. | 人类目前所直接利用的能量大部分是由化学反应产生的 | |
| B. | 人体运动所消耗的能量与化学反应无关 | |
| C. | 我国目前最主要的能源是煤炭 | |
| D. | 煤、石油、天然气是当今世界最重要的三种化石燃料 |
13.氢化钠NaH是一种白色的离子晶体,其中钠是+1价.NaH与水反应放出氢气.下列叙述中,正确的是( )
| A. | NaH在水中显酸性 | |
| B. | NaH中氢离子半径比锂离子半径大 | |
| C. | NaH中氢离子可被还原为氢气 | |
| D. | Na与其它碱金属都必须保存在煤油中 |
3.Na2CO3俗称纯碱,是基本化工原料.下列涉及Na2CO3的方程式中,正确的是( )
| A. | Na2O2与CO2反应生成Na2CO3:Na2O2+CO2═Na2CO3+O2 | |
| B. | Na2CO3溶液呈碱性:CO32-+H2O?H2CO3+OH- | |
| C. | Na2CO3溶液除去CH3COOC2H5中的CH3COOH:CO32-+2H+═CO2↑+H2O | |
| D. | 饱和Na2CO3溶液处理水垢中的CaSO4:CO32-+CaSO4═CaCO3+SO42- |
10.将一小块金属钠长期露置于空气中,最终的产物是( )
| A. | Na2CO3 | B. | Na2O | C. | NaOH | D. | Na2CO3•10H2O |
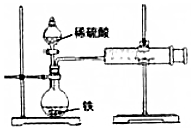 某小组的同学们利用如图装置,探究不同条件对铁与酸反应速率的影响.
某小组的同学们利用如图装置,探究不同条件对铁与酸反应速率的影响.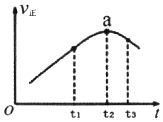 氮和硫及其化合物的转化是资源利用和环境保护的重要研究课题.
氮和硫及其化合物的转化是资源利用和环境保护的重要研究课题.