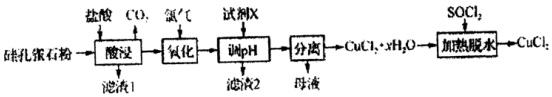
��Ŀ����
1����ͼ��һ����ȡ������������Ϊԭ�Ͻ����ض���Ӧ��װ�ã�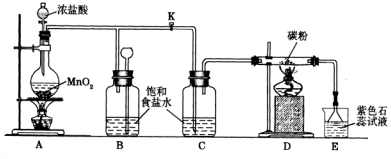
��1��A����������װ�ã����еĻ�ѧ��Ӧ����Ϊ4HCl+MnO2$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+2H2O+Cl2��������8.7g MnO2��10mol•L-1������120mL��Ӧ��ȡCl2���ڱ�״���¿�����2.24������
��2��ʵ�鿪ʼʱ���ȵ�ȼA���ľƾ��ƣ�������K����Cl2��������װ�ã��ٵ�ȼD���ƾ��ƣ�������Eװ�ã�Cl2ͨ��Cƿ���ٽ���D��Dװ�õ�Ӳ�ʲ�������ʢ��̿�ۣ�����������ԭ��Ӧ�������ΪCO2��HCl��װ��C������������Cl2�е�HCl���壬�ṩD������ˮ������
��3����E������ɫʯ����Һ����ɫ����ɫ��Ϊ��ɫ���ٱ�Ϊ��ɫ����ԭ�������ɵ�HCl����ʹ��ɫʯ����Һ��죬��δ��Ӧ���Cl2��H2O���ò�����HClO��Ư������ʹ��ɫ��ʧ��
��4������E���ձ�����Һ��Ϊ����ʯ��ˮ����Ӧ��������ΪB����ѡ���ţ�
��A���а�ɫ�������� ��B��������C�������ɰ�ɫ�����������ɫ������ʧ��
���� ��1��ʵ�����ü���Ũ������������̻�����Ʊ����������ݷ���ʽ4HCl+MnO2$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+2H2O+Cl2�� �����������������
��2���Ȼ������弫������ˮ����ˮ���ṩˮ�������ݴ˷�����
��3��������ˮ��Ӧ��������ʹ����ᣬ��������ʹ��������ʽ��
��4�����Ȼ��⡢������ͳ���ʯ��ˮ��Ӧ�����ɿ����Ե��κ�ˮ��
��� �⣺��1��Ũ��������������ڼ��������·�Ӧ�����Ȼ��̡�������ˮ������ʽ��4HCl+MnO2$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+2H2O+Cl2����
��n��MnO2��=$\frac{m}{M}$=$\frac{8.7g}{87g/mol}$=0.1mol
n��HCl��=CV=10mol•L-1��0.12L=1.2mol ���ݷ���ʽ��HCl��������ѧ����ʽ����Ӧ���Բ������Ϊ�������
��4HCl+MnO2$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+2H2O+Cl2��
1mol 22.4L
0.1mol 2.24L
�ʴ�Ϊ��4HCl+MnO2$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+2H2O+Cl2����2.24��
��2���Ȼ������弫������ˮ����ˮ���ṩˮ�������ʴ�Ϊ������Cl2�е�HCl���壬�ṩD������ˮ����
��3��������ˮ��Ӧ��������ʹ����ᣬHCl����ˮ�����ԣ�ʹ��ɫʯ����Һ���ɫ����������ˮ���ɾ���ǿ�����Ե�HClO��ʹ��Һ��ɫ�����Կ�������Ϊ��ʯ���ȱ�����ɫ��
�ʴ�Ϊ�����ɵ�HCl����ʹ��ɫʯ����Һ��죬��δ��Ӧ���Cl2��H2O���ò�����HClO��Ư������ʹ��ɫ��ʧ��
��4��ʣ���������Eװ���к�ˮ��Ӧ��������ʹ����ᣬ�Ȼ��⡢������ͳ���ʯ��ˮ��Ӧ�����ɿ����Ե��κ�ˮ�����Է�Ӧ�����������ް�ɫ�������ɣ�
�ʴ�Ϊ��B��
���� ���⿼��ʵ������ȡ�����������ʵ����ʣ���ȷ��Ӧԭ���ǽ����Ĺؼ�����Ŀ�ѶȲ���

| A�� | 1 mol������NA��һ����̼���ӵ�������� | |
| B�� | NA��O2���Ӻ�NA��O3���ӵ�������� | |
| C�� | NA��O2��NA��H2��������Ϊ16��1 | |
| D�� | ����ͬΪ16 g��O2��O3�ж����е���ԭ����Ŀ��ͬ |
| A�� | �ռҺ̬������� NaCl���ƾ� | |
| B�� | ��ʯ�ҡ����ס���ʯ�� ����NaCl��BaSO4 | |
| C�� | �ɱ��������Ȼ��� ͭ���������� | |
| D�� | ���������������� ���ڵ�KNO3��������Һ |
��Ca��OH��2����BaCl2����Na2SiO3����Ba��NO3��2���ݱ����ƣ���Na2CO3 ��
| A�� | �٢ڢۢ� | B�� | �ڢݢ� | C�� | �ۢܢݢ� | D�� | �ۢܢ� |
| A�� | �����ˮ������Һ�еμӵ�ˮ�����ɼ�������Ƿ�ˮ�� | |
| B�� | NaAlO2 ��Һ�еμ� Na2 CO3 ��Һ���г������������� | |
| C�� | �� SO2 �ֱ�ͨ�����ᱵ��Һ�����а������Ȼ�����Һ�в����ij����ɷֲ�ͬ | |
| D�� | �ò�˿պȡ������Һ������ɫ��Ӧ������ʻ�ɫ��һ����������Һ |
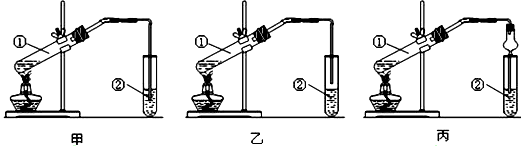
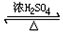 CH3COOC2H5+H2O��
CH3COOC2H5+H2O��