题目内容
5.8g硫磺在 O2中完全燃烧生成SO2气体,放出的热量是74.2KJ,则生成标准状况下的二氧化硫体积是5.6L,热化学方程式为S(s)+O2(g)=SO2(g);△H=-296.8KJ/mol.产生的SO2用NaOH溶液吸收,最少需要NaOH0.25mol.分析 热化学方程式的书写,需要注意的有:物质的状态、反应热的数值与单位,反应热的数值与化学方程式前面的系数成正比.
解答 解:8g硫粉完全燃烧生成二氧化硫气体,放出74.2kJ的热量,所以8g硫粉完全燃烧生成二氧化硫气体5.6L,放出296kJ的热量,则热化学方程式为:S(s)+O2(g)═SO2(g),△H=-296kJ/mol,最少需要NaOH0.25mol,故答案为:5.6L,S(s)+O2(g)═SO2(g),△H=-296kJ/mol,0.25mol.
点评 本题考查了热化学方程式的书写和计算,难度不大,注意掌握热化学方程式的书写规则.

练习册系列答案
 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
15.在容积固定的密闭容器中充入一定量的X、Y两种气体,一定条件下发生可逆反应:3X(g)+Y(g)?2Z(g),并达到平衡.已知正反应是放热反应,测得X的转化率为37.5%,Y的转化率为25%,下列有关叙述正确的是( )
| A. | 若X的反应速率为0.2 mol/(L•s),则Z的反应速率为0.3 mol/(L•s) | |
| B. | 若向容器中充入氦气,压强增大,Y的转化率提高 | |
| C. | 升高温度,正反应速率减小,平衡向逆反应方向移动 | |
| D. | 开始充入容器中的X、Y物质的量之比为2:1 |
16.对于以下反应:A(s)+3B(g)?2C(g)+D(g),在一定温度、体积固定的密闭容器中进行,下列叙述中能说明上述反应达到平衡状态的是( )
| A. | 混合气体的密度不随时间变化而变化 | |
| B. | 3v正(B)=v逆(D) | |
| C. | D的物质的量分数在混合气体中保持不变 | |
| D. | B、C、D的分子个数之比为3:2:1 |
10.有一可逆反应2A(g)+3B(g)?4C(g)+D(g),已知起始浓度c(A)=2mol/L,c(B)=3mol/L,c(C)=c(D)=0,反应开始20min后达到平衡状态,此时D的平衡浓度为0.5mol/L,则下列说法不正确的是( )
| A. | 前20 min的平均反应速度$\overline v$(C)=0.1 mol/(L•min) | |
| B. | A的转化率为50% | |
| C. | C的平衡浓度c(C)=4 mol/L | |
| D. | B的平衡浓度c(B)=1.0 mol/L |
14.下列烷烃的系统命名中,不正确的是( )
| A. | 3,4-二甲基戊烷 | B. | 2,3-二甲基丁烷 | ||
| C. | 2,2-二甲基丁烷 | D. | 2,2,3,3-四甲基丁烷 |
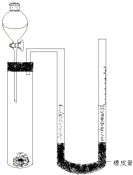 在化学研究领域,经常需要对一些物质进行性质的确定.如利用下列装置(夹持仪器已略去)测出一定质量镁与盐酸反应放出的气体体积,对金属镁的相对原子质量进行测定,实验步骤如下:
在化学研究领域,经常需要对一些物质进行性质的确定.如利用下列装置(夹持仪器已略去)测出一定质量镁与盐酸反应放出的气体体积,对金属镁的相对原子质量进行测定,实验步骤如下: