题目内容
下列离子方程式错误的是( )
| A、灭火器中盛装的是Al2(SO4)3溶液和NaHCO3溶液,使用时把两者混合即可生成CO2:Al3++3HCO3-═Al(OH)3↓+3CO2↑ |
| B、Al(OH)3电离:H2O+AlO2-+H+?Al(OH)3?Al3++3OH- |
| C、HF溶于水:HF+H2O?H3O++F- |
| D、Na2S溶于水:S2-+2H2O═H2S+2OH- |
考点:离子方程式的书写
专题:离子反应专题
分析:A.铝离子与碳酸氢根离子发生双水解生成氢氧化铝和二氧化碳;
B.氢氧化铝为两性氢氧化物存在酸式、碱式两种电离方式;
C.氢氟酸为弱电解质,电离用可逆号;
D.硫离子为多元弱酸根离子,分步水解,以第一步为主.
B.氢氧化铝为两性氢氧化物存在酸式、碱式两种电离方式;
C.氢氟酸为弱电解质,电离用可逆号;
D.硫离子为多元弱酸根离子,分步水解,以第一步为主.
解答:
解:A.灭火器中盛装的是Al2(SO4)3溶液和NaHCO3溶液,碳酸氢根离子与铝离子发生双水解反应生成二氧化碳和氢氧化铝:Al3++3HCO3-═Al(OH)3↓+3CO2↑,故A正确;
B.Al(OH)3为两性氢氧化物,存在酸式、碱式两种电离方式,电离的离子方程式:H2O+AlO2-+H+?Al(OH)3?Al3++3OH-,故B正确;
C.HF为弱电解质,溶于水发生电离,生成水合氢离子和氟离子,电离方程式:HF+H2O?H3O++F-,故C正确;
D.Na2S是多元弱酸盐溶于水发生水解,分步水解,以第一步为主,电离方程式:S2-+H2O═HS-+OH-,故D错误;
故选:D.
B.Al(OH)3为两性氢氧化物,存在酸式、碱式两种电离方式,电离的离子方程式:H2O+AlO2-+H+?Al(OH)3?Al3++3OH-,故B正确;
C.HF为弱电解质,溶于水发生电离,生成水合氢离子和氟离子,电离方程式:HF+H2O?H3O++F-,故C正确;
D.Na2S是多元弱酸盐溶于水发生水解,分步水解,以第一步为主,电离方程式:S2-+H2O═HS-+OH-,故D错误;
故选:D.
点评:本题考查了离子方程式的书写,侧重考查盐类水解和弱电解质电离,明确电解质强弱、盐类水解规律是解题关键,题目难度不大.

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
T°C时在2L密闭容器中使X(g)与Y(g)发生反应生成Z(g).反应过程中X,Y,Z的物质的量变化如图1所示;若保持其他条件不变,温度分别为T1和T2,Y的体积百分含量与时间的关系如图2所示.下列分析正确的( )
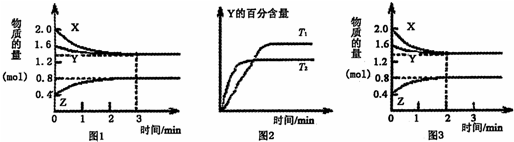

| A、容器中发生的反应可表示为:3X(g)+Y(g)?4Z(g) |
| B、0-3 min内,v(X)=0.2 mol?L-1?min-1 |
| C、若改变条件,使反应进程如图3所示,则改变的条件可能是增大压强 |
| D、其他条件不变升高温度,v正、v重都增大,且重新达到平衡前v正>v重 |
下列比较中不正确的是( )
| A、金属性:K>Na>Li |
| B、热稳定性:HI>HCl>HF |
| C、非金属性:F>O>N |
| D、碱性:NaOH>Mg(OH)2>Al(OH)3 |
下列解释事实的离子方程式不正确的是( )
| A、酸性KMnO4溶液与H2O2反应:2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O |
| B、向FeBr2溶液中通入足量氯气:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
| C、向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+ |
| D、(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-=Fe(OH)2↓ |
含铀矿物通常用铅(Pb)的同位素测年法进行断代,下列关于
Pb和
Pb说法正确的是( )
206 82 |
207 82 |
| A、含不同的质子数 |
| B、含不同的电子数 |
| C、含相同的中子数 |
| D、互相转化时不属于化学变化 |
通常状况下,下列物质所占体积最大的是( )
| A、508gI2 |
| B、16gO2 |
| C、32gHCl |
| D、3gH2 |
下列说法正确的是( )
| A、化学反应一步完成与分几步完成,反应热是不同数值 |
| B、盖斯定律解决的是化学反应过程问题 |
| C、盖斯定律在科研中的重要作用在于可以解决反应很慢或不直接发生的反应的反应热问题 |
| D、无法用盖斯定律计算反应热 |