题目内容
5.碳酸锂(相对分子质量74)广泛应用于化工、冶金、陶瓷、医药、制冷、焊接、锂合金等行业.制备流程如图: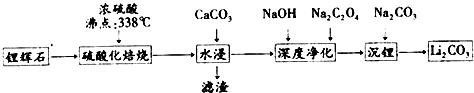
已知:碳酸锂的溶解度为(g/L)
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 80 | 100 |
| Li2CO3 | 1.54 | 1.43 | 1.33 | 1.25 | 1.17 | 1.08 | 1.01 | 0.85 | 0.72 |
(2)硫酸化焙烧工业反应温度控制在250-300℃,主要原因是温度低于250℃,反应速率较慢,温度高于300℃,硫酸挥发较多;同时,硫 酸用量为理论耗酸量的115%左右,硫酸如果加入过多则ABC(填入选项代号).
A.增加酸耗量 B.增加后续杂质的处理量 C.增加后续中和酸的负担
(3)水浸时,需要在搅拌下加入石灰石粉末的主要作用是除去多余的硫酸,同时调整pH,除去大部分杂质.
(4)“沉锂”的化学反应方程式为Na2CO3+Li2SO4=Li2CO3↓+Na2SO4
(5)“沉锂”需要在95℃以上进行,主要原因是温度越高,碳酸锂溶解度降低,可以增加产率.过滤碳酸锂所得母液 中主要含有硫酸钠,还可能含有碳酸钠和碳酸锂.
分析 由制备流程可知,锂辉石加硫酸,浸取焙烧,氧化铝、氧化锂溶解,二氧化硅不反应,水浸时加入碳酸钙,除去为反应的硫酸,同时调节溶液pH值,可以将Al3+转化为Al(OH)3沉淀,过滤除去不溶物,滤液再进行深度净化后主要为Li2SO4、Na2SO4,最后加入Na2CO3,转化为溶解度更小Li2CO3析出.
(1)将各元素写成氧化物,注意各元素原子数目比例不变;
(2)升高温度,反应速率加快,温度高于300℃时硫酸挥发;硫酸如果加入过多,消耗的酸多,后续中还需要除去过量的硫酸;
(3)加入碳酸钙除去未反应的硫酸,同时调节溶液pH值;
(4)“沉锂”过程是碳酸钠与Li2SO4反应生成Li2CO3;
(5)温度越高,碳酸锂溶解度降低,减少碳酸锂溶解;溶液中硫酸钠不反应,使用的碳酸钠要过量,少量碳酸锂溶解在溶液中.
解答 解:锂辉石加硫酸,浸取焙烧,氧化铝、氧化锂溶解,二氧化硅不反应,水浸时加入碳酸钙,除去为反应的硫酸,同时调节溶液pH值,可以将Al3+转化为Al(OH)3沉淀,过滤除去不溶物,滤液再进行深度净化后主要为Li2SO4、Na2SO4,最后加入Na2CO3,转化为溶解度更小Li2CO3析出.
(1)锂辉石(Li2Al2Si4Ox)可以用氧化物的形式表示,根据化合价代数和为0,可以确定Li2Al2Si4Ox中x=$\frac{1×2+3×2+4×4}{2}$=12,所以该化合物用氧化物的形式表示为Li2O•Al2O3•4SiO2,
故答案为:Li2O•Al2O3•4SiO2;
(2)温度低于250℃,反应速率较慢,温度高于300℃,硫酸挥发较多,反应温度控制在250-300℃,反应速率较快,避免硫酸挥发;
硫酸如果加入过多,消耗的酸多,后续中还需要除去过量的硫酸,增加后续杂质的处理量、增加后续中和酸的负担,
故答案为:温度低于250℃,反应速率较慢,温度高于300℃,硫酸挥发较多;ABC;
(3)加入碳酸钙除去未反应的硫酸,同时调节溶液pH值,除去大部分杂质,
故答案为:除去多余的硫酸,同时调整pH,除去大部分杂质;
(4)“沉锂”过程是碳酸钠与Li2SO4反应生成Li2CO3,反应方程式为:Na2CO3+Li2SO4=Li2CO3↓+Na2SO4,
故答案为:Na2CO3+Li2SO4=Li2CO3↓+Na2SO4;
(5)温度越高,碳酸锂溶解度降低,减少碳酸锂溶解,可以增加产率;溶液中硫酸钠不反应,使用的碳酸钠要过量,少量碳酸锂溶解在溶液中,过滤碳酸锂所得母液中主要含有硫酸钠,还可能含有碳酸钠、碳酸锂,
故答案为:温度越高,碳酸锂溶解度降低,可以增加产率;碳酸钠;碳酸锂.
点评 本题考查物质的制备实验,为高频考点,把握制备实验流程、物质分离提纯实验操作、对操作与原理的分析评价等为解答的关键,是对学生综合能力的考查,注意对工艺流程的理解,题目难度较大.

| A. | 浓硝酸和稀硝酸都具有氧化性 | B. | 铜与硝酸的反应属于置换反应 | ||
| C. | 硝酸可氧化Fe2+ | D. | 可用铁或铝制品盛装浓硝酸 |
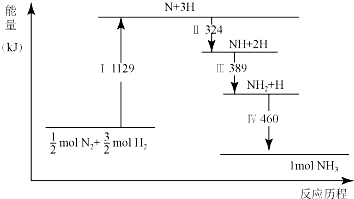
| A. | Ⅰ中破坏的均为极性键 | B. | Ⅳ中NH2与H2生成NH3 | ||
| C. | Ⅱ、Ⅲ、Ⅳ均为放热过程 | D. | N2(g)+3H2(g)?2NH3(g)△H>0 |
| A. | 麦芽糖和蔗糖 | B. | 与 CH3-CH2-CH2-CH3 与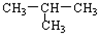 | ||
| C. | C2H6与C3H8 | D. | O2与O3 |
| A. | 2KBr+Cl2=2KCl+Br2 | B. | CaCO3=CaO+CO2↑ | ||
| C. | SO3+H2O=H2SO4 | D. | MgCl2+2NaOH=Mg(OH)2↓+NaCl |
| A. | c(HCl)>c(CH3COOH) | |
| B. | c(Cl-)=c(CH3COO-) | |
| C. | 等体积的盐酸和醋酸溶液分别与足量的Zn完全反应,盐酸产生的H2多 | |
| D. | 用同浓度的NaOH溶液分别与等体积的盐酸和醋酸溶液恰好反应完全,盐酸消耗的NaOH溶液体积多 |
| A. | 含有大量Fe2+的溶液:Na+、SO42+、NH4+、Fe(CN)63- | |
| B. | 使甲基橙变红的溶液:NH4+、CH3COO一、SO42+、Mg2+ | |
| C. | 某无色溶液:OH一、K+、ClO一、Ba2+ | |
| D. | 含有大量NO3-的溶液:K+、I一、NH4+、H+ |