题目内容
8.短周期A、B、C、D、E5种主族元素,原子序数依次增大,A是元素周期表中原子半径最小元素,B元素最高价氧化物分子式为B2O5;C的阴离子和D的阳离子具有相同的电子层结构,E的L层电子数等于K、M两个电子层上电子数之和.(1)元素:A为H,B为N
(2)E在周期表中的位置为第三周期第ⅥA族
(3)C、D两元素的单质反应,生成一种淡黄色的固体F,则F的化学式为是Na2O2,属于化合物离子(填“离子”或“共价”),该化合物中阴阳离子数比为1:2
(4)单质Cu能溶于元素B最高价氧化物对应水化物的稀溶液,请写出该反应离子方程式3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
(5)E 的一种氧化物为酸雨的“罪魁祸首”.设计一实验证明某气体为E 的该氧化物:通入品红溶液,品红褪色,加热品红恢复原来颜色,并写出该氧化物与足量NaOH的反应离子方程式SO2+2OH-=SO32-+H2O.
分析 短周期A、B、C、D、E5种主族元素,原子序数依次增大,A是元素周期表中原子半径最小元素,则A为氢元素;E的L层电子数等于K、M两个电子层上电子数之和,则E原子M层电子数为8-2=6,故E为S元素;C的阴离子和D的阳离子具有相同的电子层结构,(3)C、D两元素的单质反应,生成一种淡黄色的固体F,F为过氧化钠,C为O元素、D为Na元素;B元素最高价氧化物分子式为B2O5,则B处于VA族,且原子序数小于O,则B为氮元素.
解答 解:短周期A、B、C、D、E5种主族元素,原子序数依次增大,A是元素周期表中原子半径最小元素,则A为氢元素;E的L层电子数等于K、M两个电子层上电子数之和,则E原子M层电子数为8-2=6,故E为S元素;C的阴离子和D的阳离子具有相同的电子层结构,(3)C、D两元素的单质反应,生成一种淡黄色的固体F,F为过氧化钠,C为O元素、D为Na元素;B元素最高价氧化物分子式为B2O5,则B处于VA族,且原子序数小于O,则B为氮元素.
(1)由以上分析,可知A为H元素、B为N元素、故答案为:H;N;
(2)E为S元素,处于周期表中第三周期第ⅥA族,故答案为:第三周期第ⅥA族;
(3)C的阴离子和D的阳离子具有相同的电子层结构,C、D两元素的单质反应,生成一种淡黄色的固体F,F为Na2O2,属于离子化合物,该化合物中阴阳离子数比为1:2,
故答案为:Na2O2;离子;1:2;
(4)单质Cu溶于稀硝酸的反应离子方程式:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,
故答案为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;
(5)E 的一种氧化物为酸雨的“罪魁祸首”,该氧化物为二氧化碳,实验证明某气体为二氧化硫的方法为:通入品红溶液,品红褪色,加热品红恢复原来颜色,
二氧化硫与足量NaOH的反应离子方程式:SO2+2OH-=SO32-+H2O,
故答案为:通入品红溶液,品红褪色,加热品红恢复原来颜色;SO2+2OH-=SO32-+H2O.
点评 本题考查位置结构与性质关系的综合应用,正确推断各元素为解答关键,注意利用(3)中F为淡黄色固体推断C、D,熟练掌握元素化合物性质.

| A. | 1molCH3+(甲基碳正离子)含有的电子数目为9NA | |
| B. | 27g Al在标准状况下的22.4L Cl2中燃烧,转移的电子总数为3 NA | |
| C. | 0.2 mol•L-1的Na2CO3溶液中含有CO32-的数目一定小于0.2NA | |
| D. | 7.8gNa2S和Na2O2的混合物中含有的阴离子总数为0.1 NA |

该黑色物质可能为炭与另一种氧化物组成的混合物.
根据题意和图示回答下面问题:
(1)装置图2中A的名称坩埚.
(2)此氧化物可能是FeO或Fe3O4(写化学式).
(3)对黑色固体物质的组成作如图3所示探究
①实验I加入盐酸溶液的目的是检验黑色固体物质中是否有碳,同时溶解氧化物.
②仅通过实验Ⅱ,用最简步骤能快速确定黑色氧化物的组成,请完善该设计.(限选试剂:稀盐酸、KSCN溶液、10%H2O2溶液)
| 实验操作 | 预期现象与结论 | 相关离子方程式 |
| 取少量实验Ⅰ中的澄清溶液,加入试剂适量的KSCN溶液 | 如果溶液显红色,则黑色物质为Fe3O4,反之则为FeO | Fe3++3SCN-═Fe(SCN)3 |
| A. | Na2SO4溶液 | B. | FeCl3溶液 | C. | Cu(NO3)2溶液 | D. | 稀硫酸 |
| A. | 充电时,电解质溶液中K+向阳极移动 | |
| B. | 放电时,电解质溶液中K+向正极移动 | |
| C. | 充电时,阳极反应为:Zn(OH)${\;}_{4}^{2-}$+2e-═Zn+4OH- | |
| D. | 放电时,电路中通过2mol电子,消耗氧气22.4L(标准状况) |
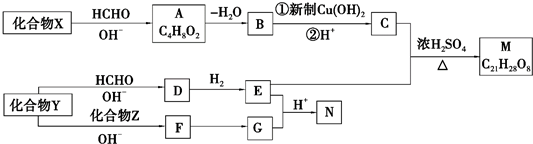
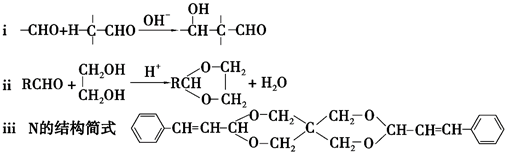
 +2Cu(OH)2+NaOH$\stackrel{△}{→}$
+2Cu(OH)2+NaOH$\stackrel{△}{→}$ +Cu2O↓+3H2O.
+Cu2O↓+3H2O. .
.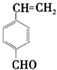 和
和 .
. Ⅰ:A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等.
Ⅰ:A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等.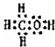 .
. .
.