题目内容
短周期主族元素,X-核外只有2个电子,则X为 .
考点:原子核外电子排布
专题:元素周期律与元素周期表专题
分析:短周期元素,X-核外只有2个电子,阴离子核外电子数=质子数+电荷数,原子中质子数=原子序数,据此判断X元素.
解答:
解:阴离子核外电子数=质子数+电荷数,原子中质子数=原子序数,短周期元素,X-核外只有2个电子,说明X原子质子数=原子序数=2-1=1,所以为H元素,
故答案为:H.
故答案为:H.
点评:本题考查元素判断,明确阴阳离子质子数计算方法是解本题关键,知道原子中原子序数与质子数关系,题目难度不大.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
反应:NaCl+CO2+NH3+H2O═NaHCO3↓+NH4Cl是“氨碱法”的重要反应,以下是对该反应涉及的有关知识的部分见解,其中不正确的是( )
| A、该条件下NaHCO3的溶解度较小 |
| B、NaHCO3不是纯碱 |
| C、析出固体后的溶液为NaHCO3的不饱和溶液 |
| D、析出晶体后的溶液为NaHCO3的饱和溶液 |
3molA和2.5molB混合于容积为2L的容器内,使它们发生反应2A(s)+3B(g)?2C(g)+D(g),经过5min生成0.5molD,下列说法正确的是( )
| A、B的平均消耗速率为0.3mol/(L?min) |
| B、C的平衡浓度为2mol/L |
| C、平衡后,增大压强,平衡将向正方向移动 |
| D、若反应容器内气体的密度不再发生变化,说明反应已经达到平衡 |
 )互为同系物.
)互为同系物.


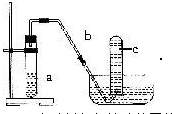
 实验室制取乙烯的装置如下图所示,请回答:
实验室制取乙烯的装置如下图所示,请回答: