题目内容
中国女药学家屠呦呦因创新发现了青蒿素而获得了2015年诺贝尔生理学或医学奖,其方法是用乙醚作为溶剂,提取青蒿中的青蒿素,这种方法的原理属于( )
A. 过滤 B. 蒸发 C. 结晶 D. 萃取
练习册系列答案
相关题目
20. 汽车尾气是导致雾霾天气的重要源头之一,其含有的NO(g)和CO(g)在一定温度和催化剂条件下可发生反应.
汽车尾气是导致雾霾天气的重要源头之一,其含有的NO(g)和CO(g)在一定温度和催化剂条件下可发生反应.
(一)已知:反应l:N2(g)+O2(g)═2NO(g)△H1 K1
反应2:CO(g)+$\frac{1}{2}$O2(g)═CO2 (g)△H2 K2
反应3:2NO(g)+2CO(g)═N2(g)+CO2(g)△H3 K3
则反应3的焓变△H3=2△H2-△H1(用△H1和△H2表示) 平衡常数K3=$\frac{{{K}_{2}}^{2}}{{K}_{1}}$(用K1和K2表示).
(二)向1.0L恒容密闭容器中,充入N2O(g)和CO(g),可发生如下反应:N2O(g)+CO(g)?N2(g)+CO2(g),所得实验数据如表:
上述实验编号①中,若10min时测得n(N2)=0.12mol,则0至10min内,用CO2表示的平均反应速率以v(CO2)=0.012mol•(L•min)-1;
(2)500℃时,欲使N2O的平衡转化率a(N2O)≥80%,则起始时n(N2O):n(CO)≤1:4.
(3)上述实验编号④达平衡时,b<0.24(填“>”、“<”或“=”),原因是该反应△H<0,升高温度,平衡向逆反应方向移动,故b<0.24mol.
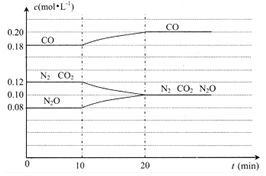
(4)N2O(g)+CO(g)?N2(g)+CO2(g)的反应体系达到平衡后,各物质的浓度在不同条件下的变化情况如如图所示:
①若在第10min仅改变了一个条件,第20min时是在新条件下达到新的平衡状态,则第10min 时改变的条件可能是升温;
②比较CO在第5min和第25min时速率的大小v(5)<v(25)(填”>”、“<”或“=”),你判断的理由是相对于第5min而言,在第10min时升高了温度,且浓度增加了,在其它条件不变时,速率会变快.
 汽车尾气是导致雾霾天气的重要源头之一,其含有的NO(g)和CO(g)在一定温度和催化剂条件下可发生反应.
汽车尾气是导致雾霾天气的重要源头之一,其含有的NO(g)和CO(g)在一定温度和催化剂条件下可发生反应.(一)已知:反应l:N2(g)+O2(g)═2NO(g)△H1 K1
反应2:CO(g)+$\frac{1}{2}$O2(g)═CO2 (g)△H2 K2
反应3:2NO(g)+2CO(g)═N2(g)+CO2(g)△H3 K3
则反应3的焓变△H3=2△H2-△H1(用△H1和△H2表示) 平衡常数K3=$\frac{{{K}_{2}}^{2}}{{K}_{1}}$(用K1和K2表示).
(二)向1.0L恒容密闭容器中,充入N2O(g)和CO(g),可发生如下反应:N2O(g)+CO(g)?N2(g)+CO2(g),所得实验数据如表:
| 实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
| n(N2O) | n(CO) | n(CO2) | ||
| ① | 400 | 0.20 | 0.30 | 0.14 |
| ② | 500 | 0.10 | 0.40 | 0.080 |
| ③ | 500 | 0.30 | 0.20 | A |
| ④ | 600 | 0.60 | 0.40 | B |
(2)500℃时,欲使N2O的平衡转化率a(N2O)≥80%,则起始时n(N2O):n(CO)≤1:4.
(3)上述实验编号④达平衡时,b<0.24(填“>”、“<”或“=”),原因是该反应△H<0,升高温度,平衡向逆反应方向移动,故b<0.24mol.
(4)N2O(g)+CO(g)?N2(g)+CO2(g)的反应体系达到平衡后,各物质的浓度在不同条件下的变化情况如如图所示:
①若在第10min仅改变了一个条件,第20min时是在新条件下达到新的平衡状态,则第10min 时改变的条件可能是升温;
②比较CO在第5min和第25min时速率的大小v(5)<v(25)(填”>”、“<”或“=”),你判断的理由是相对于第5min而言,在第10min时升高了温度,且浓度增加了,在其它条件不变时,速率会变快.
1.部分有机物分子会产生互变异构,如苯与棱晶烷、降冰片二烯与四环烷均能发生互变异构体:

棱晶烷和四环烷的二氯代物的同分异构体数目分别为( )

棱晶烷和四环烷的二氯代物的同分异构体数目分别为( )
| A. | 2,7 | B. | 2,8 | C. | 3,7 | D. | 3,8 |