题目内容
20.反应2A(g)+B(g)?3C(g),起始时按5:2的体积比把A、B两气体混合后,充入一体积不变的密闭容器中,在恒定温度下使之反应,达平衡时混合气体中C的体积分数为60%.(已知A、B的相对分子质量分别为a、b)求:(1)A的转化率
(2)平衡时混合气体的平均相对分子质量.
(3)平衡时压强与起始时相比,有何变化?
分析 反应开始时A、B的体积之比为5:2,设反应起始时A、B物质的量分别是5mol、2mol,该反应前后气体的物质的量不变,故达到平衡时混合气体为7mol,平衡时C的体积分数是60%,故n(C)=(5+2)mol×60%=4.2mol,
(1)根据方程式知,参加反应的△n(A)=$\frac{2}{3}$△n(C)=$\frac{2}{3}$=2.8mol,转化率=$\frac{物质的量变化量}{起始物质的量}$×100%;
(2)根据质量守恒定律,可知平衡时混合气体总质量等于起始时A、B质量之和,根据$\overline{M}$=$\frac{{m}_{总}}{{n}_{总}}$计算平均相对分子质量;
(3)恒温恒容条件下,气体的压强之比等于物质的量之比.
解答 解:(1)反应开始时A、B的体积之比为5:2,设反应起始时A、B物质的量分别是5mol、2mol,该反应前后气体的物质的量不变,故达到平衡时混合气体为7mol,平衡时C的体积分数是60%,故n(C)=(5+2)mol×60%=4.2mol,根据方程式知,参加反应的△n(A)=$\frac{2}{3}$△n(C)=$\frac{2}{3}$×4.2mol=2.8mol,故A的转化率=$\frac{2.8mol}{5mol}$×100%=56%,
答:A的转化率为56%;
(2)根据质量守恒定律,可知平衡时混合气体总质量等于起始时A、B质量之和,故混合气体总质量为(5a+2b)g,则平均摩尔质量为$\frac{(5a+2b)g}{7mol}$=$\frac{5a+2b}{7}$g/mol,故平均相对分子质量为$\frac{5a+2b}{7}$g/mol,
答:平均相对分子质量为$\frac{5a+2b}{7}$;
(3)恒温恒容条件下,气体的压强之比等于物质的量之比,反应前后气体的物质的量不变,则压强不变,答:平衡时压强与起始时相比,压强不变.
点评 本题考查化学平衡有关计算,侧重考查学生分析及计算能力,明确反应中气体物质的量不变是解本题关键,题目难度不大.

 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案| A. | Cu2++2OH-=Cu(OH)2↓ CuCO3+2NaOH═Cu(OH)2↓+Na2CO3 | |
| B. | CO32-+2H+=CO2↑+H2O BaCO3+2HCl═BaCl2+CO2↑+H2O | |
| C. | Ca2++CO32-=CaCO3↓ Ca(NO3)2+Na2CO3═CaCO3↓+2NaNO3 | |
| D. | H++OH-=H2O 2KOH+H2SO4═K2SO4+2H2O |
 已知某温度下:
已知某温度下:反应①:CO2(g)+H2(g)?CO(g)+H2O(g),△H=+41.2kJ/mol;
反应②:
 (g)?
(g)? (g)+H2(g),△H=+117.6kJ/mol.
(g)+H2(g),△H=+117.6kJ/mol.①、②的化学反应平衡常数分别为K1、K2.
(1)请写出二氧化碳氧化乙苯制备苯乙烯的热化学反应方程式CO2(g)+
 (g)?
(g)? (g)+CO(g)+H2O(g)△H=+158.8 kJ/mol.该反应的化学平衡常数K=K1•K2(用K1、K2表示).
(g)+CO(g)+H2O(g)△H=+158.8 kJ/mol.该反应的化学平衡常数K=K1•K2(用K1、K2表示).(2)恒温恒容条件下,反应①达到平衡后,t1时刻通入少量CO2.请画出t1之后的正逆反应曲线,并作出标注.
(3)一定条件下,某密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.50mol/L、c(N2O4)=0.125mol/L,则2NO2(g)═N2O4(g)的平衡常数K=0.5(写出计算结果);若NO2起始浓度为2mol/L,在相同条件下反应达到平衡时,NO2的转化率为50%.
(4)在一定体积的密闭容器中,进行如下化学反应:
CO2(g)+H2(g)═CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表:
| T/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
①该反应为吸热反应(填“吸热”、“放热”).
②能使该反应的反应速率增大,且平衡向正反应方向移动的是BC.
A.及时分离出CO气体 B.适当升高温度
C.增大CO2的浓度 D.选择高效催化剂.
(1)某同学利用该反应探究浓度对反应速率的影响.实验时均加入1mL淀粉溶液做指示剂,若不经计算,直接通过褪色时间的长短判断浓度与反应速率的关系,下列试剂中应选择②③④(填序号).
①1mL 0.01mol•L-1的碘水 ②1mL 0.001mol•L-1的碘水 ③4mL 0.01mol•L-1的Na2S2O3溶液 ④4mL 0.001mol•L-1的Na2S2O3溶液
(2)若某同学选取①③进行实验,测得褪色时间为4s,计算v(S2O${\;}_{3}^{2-}$)=8.33×10-4mol/(L•s).
(3)所需的氢气可用煤和水作原料经多步反应制得,其中的一步反应为:CO(g)+H2O(g)?CO2(g)+H2(g)△H<0,200℃时,该反应的平衡常数为$\frac{1}{2.25}$,该温度下,将一定量的CO和H2投入某10L密闭容器,5min时达平衡,各物质浓度(mol
•L-1)变化如表:
| 0min | 5min | 10min | |
| CO | 0.01 | 0.0056 | |
| H2O | 0.01 | 0.0156 | |
| CO2 | 0 | 0.0044 | |
| H2 | 0 | 0.0044 |
②CO的平衡转化率为40%.
③若5min~10min只改变了某一条件,该条件是增大水蒸气的浓度,如何改变的增大0.01mol/L.
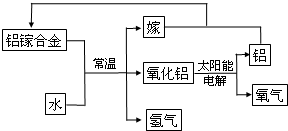 铝是地壳中含量最多的金属元素,其单质和化合物广泛应用于日常生活中.
铝是地壳中含量最多的金属元素,其单质和化合物广泛应用于日常生活中.