题目内容
17.X、Y、Z 均为短周期元素,X、Y 处于同一周期,X、Z 的最低价离子分别为X2-和Z-,Y+和Z-具有相同的电子层结构.下列说法正确的是( )| A. | 气态氢化物的稳定性:HX>HZ | B. | 原子半径:Y>X>Z | ||
| C. | 离子半径:X2->Y+>Z- | D. | 元素的最高化合价:Z>X>Y |
分析 X、Y、Z均是短周期元素,X、Z的最低价离子分别为X2-和Z-,则X为第ⅥA族元素,Z为ⅦA族元素;Y+和Z-具有相同的电子层结构,则Y在Z的下一周期,则Y为Na元素,Z为F元素,X、Y同周期,则X为S元素.
A.非金属性越强,对应氢化物越稳定;
B.同周期自左而右原子半径减小,同主族自上而下原子半径增大;
C.电子层结构相同,核电荷数越大离子半径越小,电子层越多离子半径越大;
D.F元素没有最高正化合.
解答 解:X、Y、Z均是短周期元素,X、Z的最低价离子分别为X2-和Z-,则X为第ⅥA族元素,Z为ⅦA族元素;Y+和Z-具有相同的电子层结构,则Y在Z的下一周期,则Y为Na元素,Z为F元素,X、Y同周期,则X为S元素.
A.非金属性S<F,故氢化物稳定性H2S<HF,故A错误;
B.同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径Y(Na)>X(S)>Z(F),故B正确;
C.电子层结构相同,核电荷数越大离子半径越小,电子层越多离子半径越大,故离子半径:S2->F->Na+,故C错误;
D.F元素没有最高正化合,故D错误,
故选B.
点评 本题考查原子结构与元素周期律的关系,侧重于学生的分析能力的考查,题目难度不大,关键是根据原子结构特点正确推断元素的种类.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
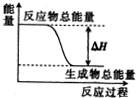
4.下列各物质间的反应,其能量变化符合右图的是( )

| A. | 灼热的碳与二氧化碳反应 | |
| B. | 碳酸钙的分解 | |
| C. | Ba(OH)2•8H2O晶体和NH4Cl晶体混合 | |
| D. | 葡萄糖在人体中转化成二氧化碳和水 |
8.设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1mol苯乙烯(C6H5CH=CH2)中含有的碳碳双键数目为4NA | |
| B. | 加热条件下,MnO2与浓盐酸反应生成7.1gCl2,转移的电子数目为0.2NA | |
| C. | 标准状况下,11.2LCCl4中含有的分子数目为0.5NA | |
| D. | 常温下,1L0.1mol•L-1的CH3COOH溶液中含有的H+数目为0.1NA |
12.设NA表示阿伏伽德罗常数的值,下列结论中正确的是( )
| A. | 25℃时,pH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA | |
| B. | 粗铜精炼时,当阳极质量减少6.4 g时,电路中转移的电子数一定不是0.2NA | |
| C. | 含0.2 mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1NA | |
| D. | 200 mL 0.5 mol•L-1 Na2CO3溶液中,由于CO32-水解,所以阴离子的数目小于0.1NA |
9.既能与盐酸反应又能与氢氧化钠溶液反应的物质组合是( )
①铝 ②氧化铁 ③氧化铝 ④碳酸氢钠 ⑤碳酸钠 ⑥偏铝酸钠.
①铝 ②氧化铁 ③氧化铝 ④碳酸氢钠 ⑤碳酸钠 ⑥偏铝酸钠.
| A. | ①③⑥ | B. | ①③④⑤ | C. | ①②③ | D. | ①③④ |
7.将足量CO2气体通入水玻璃中,然后加热蒸干,再在高温下充分燃烧,最后所得的固体物质是( )
| A. | 硅酸钠 | B. | 碳酸钠,硅酸钠 | C. | 碳酸钠,二氧化硅 | D. | 二氧化硅 |


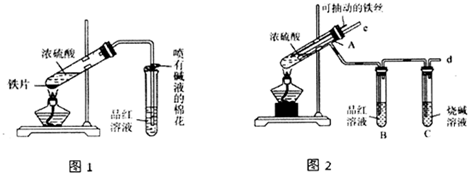
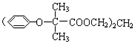 ,可用于降低血液中的胆固醇,该物质合成线路如图所示:
,可用于降低血液中的胆固醇,该物质合成线路如图所示: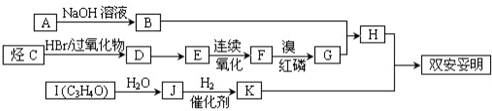
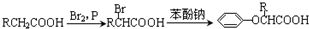
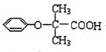 .
. .
.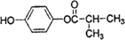 (写结构简式).
(写结构简式).