题目内容
1.下列关于物质的分离,提纯实验中的一些操作或做法,其中正确的是( )| A. | 在组装蒸馏装置时,温度计的水银球应伸入液面下 | |
| B. | 用96%的工业酒精制取无水乙醇,可采用的方法是加生石灰,再蒸馏 | |
| C. | 要除去乙烷中混有的乙烯气体可将混合气体通过盛有酸性高猛酸钾溶液的洗气瓶 | |
| D. | 用分液漏斗可以分离溴和CCl4、苯和水、乙酸和乙醇等液体混合物 |
分析 A.蒸馏时测定馏分的温度;
B.加CaO与水反应后,增大与乙醇的沸点差异;
C.乙烯被高锰酸钾氧化生成二氧化碳;
D.乙酸和乙醇互溶,不分层.
解答 解:A.蒸馏时测定馏分的温度,则温度计水银球在烧瓶支管口处,故A错误;
B.加CaO与水反应后,增大与乙醇的沸点差异,然后蒸馏可分离,故B正确;
C.乙烯被高锰酸钾氧化生成二氧化碳,引入新杂质,应利用溴水、洗气除杂,故C错误;
D.乙酸和乙醇互溶,不分层,不能利用分液漏斗分离,故D错误;
故选B.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异及发生的反应为解答的关键,注意有机物性质的综合应用,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 常温常压下,22.4L乙烯中C-H键数为4NA | |
| B. | 1L 0.1mol•L-1乙酸溶液中H+数为0.1NA | |
| C. | 室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA | |
| D. | 标准状况下,22.4L 甲醇中含有的氧原子数为1.0NA |
9.表示一个原子在第三个电子层上有10个电子可以写成( )
| A. | 3s10 | B. | 3d10 | C. | 3s23p63d2 | D. | 3s23p53d3 |
16.向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液.下列对此现象说法正确的是( )
| A. | 沉淀溶解后,将生成深蓝色的配合离子[Cu(NH3)4]2+ | |
| B. | 在[Cu(NH3)4]2+离子中,Cu2+给出孤对电子,NH3提供空轨道 | |
| C. | 上述现象说明[Cu(NH3)4]2+不如Cu(OH)2稳定 | |
| D. | 反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变 |
6.下列排列顺序正确的是( )
①热稳定性:H2O>HF>H2S
②原子半径:Na>Mg>O
③熔点:SO3>SiO2>CO2
④结合质子能力:OH->CH3COO->Cl-.
①热稳定性:H2O>HF>H2S
②原子半径:Na>Mg>O
③熔点:SO3>SiO2>CO2
④结合质子能力:OH->CH3COO->Cl-.
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ②③ |
10.烯烃R-CH═CH-R′在过量的酸性高锰酸钾溶液存在下,可氧化成RCOOH和R′COOH.现有分子式为C6H12的链烃,用过量的酸性高锰酸钾氧化生成两种不同的羧酸,则该烃的结构简式为(己知R′≠H)( )
| A. | CH2═CH-CH2CH2CH2CH3 | B. | CH3CH2CH═CHCH2CH3 | ||
| C. | CH3CH═CHCH2CH2CH3 | D. | 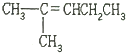 |
11.将KCl和KBr混合物13.4g溶于水配成500mL溶液,通入过量Cl2,反应后将溶液蒸干得固体11.175g,则原所配溶液中K+、Cl-、Br-的物质的量浓度之比为( )
| A. | 3:2:1 | B. | 1:2:3 | C. | 1:3:2 | D. | 3:1:1 |
 某学习小组推测SO2能与强氧化剂Cl2反应生成SO2Cl2,为此进行探究.
某学习小组推测SO2能与强氧化剂Cl2反应生成SO2Cl2,为此进行探究.