题目内容
 含氯消毒剂和过氧化物等强氧化性消毒剂可用于环境杀菌消毒.
含氯消毒剂和过氧化物等强氧化性消毒剂可用于环境杀菌消毒.(1)过碳酸钠是-种有多种用途的新型氧系固态漂白剂,化学式可表示为Na2CO3?3H2O2,它具有Na2CO3和H2O2的双重性质.
①H2O2有时可作为矿业废液消毒剂,如消除采矿业废液中的氰化物(如NaCN),经以下反应实现:NaCN+H2O2+H2O═A+NH3↑,则生成物A的化学式为
②某强酸性反应体系中,反应物和生成物共六种物质:O2、MnO4-、H2O、Mn2+、H2O2、H+.已知该反应中H2O2只发生了如下过程:H2O2→O2.写出该反应的离子方程式:
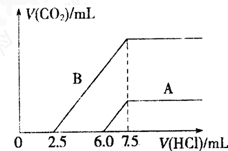
(2)某天然碱的化学式可表示为:aNa2CO3?bNaHCO3?2H2O,取m g天然碱溶于水配成溶液,再向溶液中逐滴加入1mol/L的盐酸,根据标准状况下产生的CO2的体积与所加盐酸体积之间的关系,某同学作出了如图所示的A和B曲线,试回答下列问题:
①
②加盐酸后产生CO2气体体积(标准状况)的最大值为
(3)漂白剂亚氯酸钠(NaClO2)在常温与黑暗处可保存一年.亚氯酸不稳定可分解,反应的离子方程式为:HClO2→ClO2↑+H++Cl-+H2O(未配平).在该反应中,当有1mol ClO2生成时转移的电子个数是
(4)ClO2可以用作环境杀菌消毒,ClO2的单位质量消毒效率是Cl2的
考点:化学方程式的有关计算,氯、溴、碘及其化合物的综合应用,钠的重要化合物
专题:计算题,元素及其化合物
分析:(1)①由元素守恒和原子守恒确定产物,根据双氧水的产物是否对环境有影响判断;
②由H2O2→O2知,双氧水在反应中作还原剂,所以还必须有氧化剂参加反应,在反应中得电子化合价降低,根据化合价知,高锰酸根离子作氧化剂,还原产物是锰离子,同时反应后生成水,据此写出离子方程式;
(2)①依据图象分析,开始无二氧化碳气体生成,是碳酸钠和盐酸反应生成碳酸氢钠的过程,当碳酸钠全部转化为碳酸氢钠后,再加入盐酸和碳酸氢钠反应生成二氧化碳气体,依据化学方程式计算得到样品中碳酸钠和碳酸氢钠物质的量对AB图象分析判断;
②根据计算出的碳酸钠和碳酸氢钠物质的量计算生成二氧化碳气体体积;
(3)根据化合价变化来计算转移的电子数;
(4)1molCl2可以获得2mol电子,1molClO2可以获得电子5mol电子,以此进行计算.
②由H2O2→O2知,双氧水在反应中作还原剂,所以还必须有氧化剂参加反应,在反应中得电子化合价降低,根据化合价知,高锰酸根离子作氧化剂,还原产物是锰离子,同时反应后生成水,据此写出离子方程式;
(2)①依据图象分析,开始无二氧化碳气体生成,是碳酸钠和盐酸反应生成碳酸氢钠的过程,当碳酸钠全部转化为碳酸氢钠后,再加入盐酸和碳酸氢钠反应生成二氧化碳气体,依据化学方程式计算得到样品中碳酸钠和碳酸氢钠物质的量对AB图象分析判断;
②根据计算出的碳酸钠和碳酸氢钠物质的量计算生成二氧化碳气体体积;
(3)根据化合价变化来计算转移的电子数;
(4)1molCl2可以获得2mol电子,1molClO2可以获得电子5mol电子,以此进行计算.
解答:
解:(1)①由反应NaCN+H2O2+H2O═A+NH3↑,根据质量守恒定律可知,元素守恒、原子守恒,则A的化学式为NaHCO3,故答案为:NaHCO3;
②MnO4-具有氧化性,H2O2具有还原性,H2O2只发生了如下过程:H2O2→O2,则还原反应为MnO4-→Mn2+,并由质量守恒定律及电荷守恒可知,离子反应为2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O,
故答案为:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O;
(2)①图象分析可知B图象:碳酸钠生成碳酸氢钠消耗盐酸2.5ml,碳酸氢钠生成二氧化碳消耗盐酸7.5ml-2.5ml=5ml,Na2CO3+HCl═NaHCO3+NaCl,NaHCO3+HCl═NaCl+CO2+H2O,则碳酸钠物质的量=0.0025L×1mol/L=0,0025mol,原混合物中的碳酸氢钠物质的量=0.005L×1mol/L-0.0025mol=0.0025mol,图象B合理,样品中碳酸钠和碳酸氢钠物质的量之比为1:1,天然碱的化学式为:Na2CO3?NaHCO3?2H2O;
图象A分析:碳酸钠生成碳酸氢钠消耗盐酸0.006ml,碳酸氢钠生成二氧化碳消耗盐酸7.5ml-6.0ml=1.5ml,Na2CO3+HCl═NaHCO3+NaCl,NaHCO3+HCl═NaCl+CO2+H2O,则碳酸钠物质的量=0.006L×1mol/L=0.006mol,原混合物中的碳酸氢钠物质的量=0.0015L×1mol/L-0.006mol<0,所以图象A不符合反应过程的定量关系,故A不合理;
故答案为:B;Na2CO3?NaHCO3?2H2O;
②依据计算图象B可知碳酸钠物质的量=0.0025mol,碳酸氢钠物质的量=0.0025mol,根据碳元素守恒得到最大量生成二氧化碳物质的量=0.005mol,标准状况生成二氧化碳体积=0.005mol×22.4L/mol=0.112L=112mL,故答案为:112;
(3)由HClO2→ClO2↑+H++Cl-+H2O可知,反应物中Cl元素的化合价既升高又降低,当有1molClO2生成时,转移的电子数为1mol×(4-3)×NAmol-1=NA,即为6.02×1023,
故答案为:6.02×1023;
(4)设质量都是71g,氯气得到的电子数为
×2×1=2mol,ClO2得到的电子数为
×1×5=
mol=
mol,则ClO2消毒的效率是Cl2的倍数为
=
≈2.63,故答案为:2.63;
②MnO4-具有氧化性,H2O2具有还原性,H2O2只发生了如下过程:H2O2→O2,则还原反应为MnO4-→Mn2+,并由质量守恒定律及电荷守恒可知,离子反应为2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O,
故答案为:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O;
(2)①图象分析可知B图象:碳酸钠生成碳酸氢钠消耗盐酸2.5ml,碳酸氢钠生成二氧化碳消耗盐酸7.5ml-2.5ml=5ml,Na2CO3+HCl═NaHCO3+NaCl,NaHCO3+HCl═NaCl+CO2+H2O,则碳酸钠物质的量=0.0025L×1mol/L=0,0025mol,原混合物中的碳酸氢钠物质的量=0.005L×1mol/L-0.0025mol=0.0025mol,图象B合理,样品中碳酸钠和碳酸氢钠物质的量之比为1:1,天然碱的化学式为:Na2CO3?NaHCO3?2H2O;
图象A分析:碳酸钠生成碳酸氢钠消耗盐酸0.006ml,碳酸氢钠生成二氧化碳消耗盐酸7.5ml-6.0ml=1.5ml,Na2CO3+HCl═NaHCO3+NaCl,NaHCO3+HCl═NaCl+CO2+H2O,则碳酸钠物质的量=0.006L×1mol/L=0.006mol,原混合物中的碳酸氢钠物质的量=0.0015L×1mol/L-0.006mol<0,所以图象A不符合反应过程的定量关系,故A不合理;
故答案为:B;Na2CO3?NaHCO3?2H2O;
②依据计算图象B可知碳酸钠物质的量=0.0025mol,碳酸氢钠物质的量=0.0025mol,根据碳元素守恒得到最大量生成二氧化碳物质的量=0.005mol,标准状况生成二氧化碳体积=0.005mol×22.4L/mol=0.112L=112mL,故答案为:112;
(3)由HClO2→ClO2↑+H++Cl-+H2O可知,反应物中Cl元素的化合价既升高又降低,当有1molClO2生成时,转移的电子数为1mol×(4-3)×NAmol-1=NA,即为6.02×1023,
故答案为:6.02×1023;
(4)设质量都是71g,氯气得到的电子数为
| 71g |
| 71g/mol |
| 71g |
| 67.5g/mol |
| 71×5 |
| 67.5 |
| 71 |
| 13.5 |
| 71 | ||
|
| 71 |
| 27 |
点评:本题考查了物质性质的实验探究方法和实验现象分析,反应的离子方程式书写,图象分析的计算判断,氧化还原反应电子转移数计算应用,为高频考点,侧重于学生的分析能力和计算能力的考查,注意把握氧化还原反应中转移的电子数的计算,题目难度中等.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案
相关题目