题目内容
有反应:4Zn+10HNO3(极稀过量)→4Zn(NO3)2+NH4NO3+3H2O
(1)该反应的氧化产物是 ,被还原的元素是 ;
(2)反应中HNO3的作用是 (填序号)
a. 氧化剂 b.催化剂 c.脱水剂 d.酸
(3)若有0.1mol NH4NO3生成,转移电子 NA个.
(4)若有1mol HNO3参加反应,被还原的HNO3为 mol.
(1)该反应的氧化产物是
(2)反应中HNO3的作用是
a. 氧化剂 b.催化剂 c.脱水剂 d.酸
(3)若有0.1mol NH4NO3生成,转移电子
(4)若有1mol HNO3参加反应,被还原的HNO3为
考点:氧化还原反应,氧化还原反应的计算
专题:氧化还原反应专题
分析:反应4Zn+10HNO3(稀)=4Zn(NO3)2+NH4NO3+3H2O中,Zn元素化合价升高,被氧化,N元素化合价降低,由+5价降低到-3价,结合元素化合价的变化和反应的化学方程式解答该题.
解答:
解:(1)Zn元素化合价升高,被氧化,Zn( N03)2为氧化产物,N元素化合价降低,由+5价降低到-3价,故答案为:Zn( N03)2;N;
(2)反应中N元素化合价降低,硝酸表现为氧化性,有盐生成,说明硝酸还表现为酸性,故答案为:a d;
(3)若有0.1mol NH4NO3生成,转移电子的物质的量为0.1mol×(5-(-3))=0.8mol,则转移电子0.8NA个,
故答案为:0.8NA;
(4)由方程式可知,当有10mol硝酸参加反应时,有1mol硝酸铵生成,则有1mol硝酸被还原,则若有1mol HNO3参加反应,被还原的HNO3为0.1mol.
故答案为:0.1.
(2)反应中N元素化合价降低,硝酸表现为氧化性,有盐生成,说明硝酸还表现为酸性,故答案为:a d;
(3)若有0.1mol NH4NO3生成,转移电子的物质的量为0.1mol×(5-(-3))=0.8mol,则转移电子0.8NA个,
故答案为:0.8NA;
(4)由方程式可知,当有10mol硝酸参加反应时,有1mol硝酸铵生成,则有1mol硝酸被还原,则若有1mol HNO3参加反应,被还原的HNO3为0.1mol.
故答案为:0.1.
点评:本题考查氧化还原反应,为高考高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念和电子转移的考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
以油类为溶剂的防锈漆称为油基防锈漆,由于环保方面的原因,目前要推广使用水基防锈漆,但水基漆较易溶解O2,在干燥之前易导致金属表面产生锈斑,为此要在水基漆中加入缓蚀剂,以下可作为缓蚀剂添加的是( )
| A、KMnO4 |
| B、NaNO3 |
| C、FeSO4 |
| D、HNO3 |
下列各项中的两个量,其比值一定为2:1的是( )
| A、在反应2FeCl3+Fe=3FeCl2中氧化产物与还原产物的质量比 |
| B、平均相对分子质量为34的混合气体中N2和NO2的体积比 |
| C、在密闭容器中,N2+3H2═2NH3已达平衡时NH3与N2的浓度比 |
| D、在12C16O2分子中的中子数和质子数之比 |
近年来用红外激光技术研究液氢时,发现分子间作用力也可引起微粒间的反应,在液氢中氢分子和质子形成的H3+离子,其构型是等边三角形,属于二电子三中心离子,同时H3+还可进一步形成Hn+,下列判断不正确的是( )
A、H3+的电子式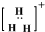 |
| B、H3+可在液氢中形成H4+、H5+、H6+ |
| C、H3+可在液氢中形成H5+、H7+、H9+ |
| D、每个H3+微粒中含有3个质子 |