题目内容
8.(1)请用下面的A-D字母填空:①乙酸乙酯制备A;②乙醛的银镜反应C;③石油分馏B;④苯酚溶液与FeCl3溶液D:A.直接加热;B.垫石棉网加热;C.水浴加热;D.不需要加热.(2)下列叙述正确的是BE(填序号)
A.向碘水中加入酒精,萃取碘水中的碘
B.液化石油气、汽油和石蜡的主要成分都是碳氢化合物
C.用水解后的淀粉溶液做银镜反应,若有银镜产生,则证明淀粉部分水解
D.将无水乙醇和浓硫酸按体积比1:3混合,加热至140℃制取乙烯
E.为证明溴乙烷分子中溴元素的存在,可向溴乙烷中加入NaOH溶液,加热;加入稀硝酸至溶液呈酸性,滴入AgNO3溶液看是否有淡黄色沉淀.
分析 (1)制取乙酸乙酯的反应在试管中进行,可以对试管直接加热;乙醛的银镜反应温度不宜过高,需要在水浴中反应;而石油的蒸馏需要在蒸馏烧瓶中进行,给蒸馏烧瓶加热需要垫上石棉网,苯酚和氯化铁溶液常温反应,据此进行解答;
(2)A.酒精与水互溶,不能使用酒精萃取碘水中的碘;
B.液化石油气、汽油和石蜡都是石油产品,石油是烃类组成的化合物;
C.有银镜产生,则证明淀粉已经水解,若证明淀粉是否完全水解,需要加入碘水检验;
D.乙醇的消去反应,温度应该控制在170℃,若140℃生成的是乙醚;
E.溴乙烷在氢氧化钠的水溶液中加热发生水解反应,加入硝酸银溶液前需要加入酸溶液中和溶液至溶液为酸性.
解答 解:①乙酸乙酯的制备中,反应在试管中进行,可以直接给试管中的混合液体加热,所以A正确,
故答案为:A;
②乙醛的银镜反应中,反应温度不宜过高,需要在控制反应温度,所以需要水浴加热,
故答案为:C;
③石油的分馏操作中,用于加热的反应装置为蒸馏烧瓶,给蒸馏烧瓶加热时需要垫上石棉网,
故答案为:B;
④苯酚溶液与FeCl3溶液常温下反应生成紫色溶液,
故答案为:D;
(2)A.由于酒精与原溶液的溶剂水互溶,无法通过酒精萃取碘水中的碘,故A错误;
B.液化石油气、汽油和石蜡都是石油产品,石油是烃类组成的化合物;液化石油气、汽油和石蜡的主要成分都是碳氢化合物,故B正确;
C.用水解后的淀粉溶液做银镜反应,若有银镜产生,则证明淀粉已经水解,无法证明淀粉完全分解;若证明淀粉是否完全水解,需要加入碘水进行检验,故C错误;
D.用酒精和浓硫酸制取乙烯时,浓硫酸的体积和酒精体积的比=3:1,加热温度是170℃,如果加热温度是140℃就生成乙醚,故D错误;
E.为证明溴乙烷分子中溴元素的存在,可向溴乙烷中加入NaOH溶液加热,溴乙烷发生水解反应生成溴离子,加入稀硝酸至溶液呈酸性后,再滴入AgNO3溶液看是否有淡黄色沉淀,该操作合理,故E正确;
故选BE.
点评 本题考查了乙酸乙酯的制取、石油的分馏、乙醛的有机反应等知识,题目难度中等,试题涉及的知识点较多,注意掌握化学实验基本操作方法,试题培养了学生灵活应用所学知识的能力.

| A. | 葡萄糖与果糖、淀粉和纤维素分别为同分异构体 | |
| B. | 若某有机物在氧气中充分燃烧生成CO2和H2O物质的量相等,则该有机物是乙烯 | |
| C. | 燃烧乙烷、环丙烷(C3H6)混合气体,所产生的CO2的量一定小于燃烧相同质量的丙烯所产生的CO2 | |
| D. | 相同质量的乙烯和乙醇在氧气中充分燃烧,消耗的氧气相等 |
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
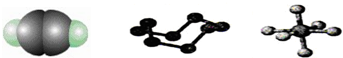
| A. | 32 g S8分子中含有0.125 mol σ键 | |
| B. | SF6是由极性键构成的非极性分子 | |
| C. | 1 mol C2H2分子中有3 mol σ键和2 mol π键 | |
| D. | 1 mol S8中含有8 mol S-S键 |
| A. | 溶液的PH增大 | B. | 溶液中的Zn2+浓度增大 | ||
| C. | 溶液中的SO42- 浓度增大 | D. | 溶液的密度增大 |
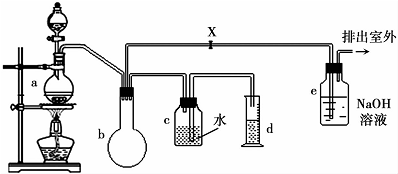
已知一氯甲烷的部分性质如下:
| 名称 | 熔点 | 沸点 | 溶解性 |
| 一氯甲烷 | -97.73℃ | -24.2℃ | 18℃时在水中微溶,与乙醚、丙酮或苯互溶,能溶于乙醇 |
(1)与甲烷氯化法相比,甲醇氯化法的优点是基本无副产品,原子利用率高.
(2)a中ZnCl2,由于加量过少仍需再加沸石以防暴沸,如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是b(填正确答案标号).
a.立即补加 b.冷却后补加 c.不需补加 d.重新配料
(3)装置b仪器的名称圆底烧瓶,作用是防止倒吸、贮气、作安全瓶等.
(4)甲烷氯化法副产物CCl4与水混合后用分液漏斗分离,CCl4从下口放出(填“上口倒出”或“下口放出”).
(5)检验气体产物CH3Cl的方法是在e的逸出口点燃CH3Cl气体,火焰呈蓝绿色(与其它烃燃烧现象有明显区别).CH3Cl燃烧的化学方程式是2CH3Cl+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+2HCl+2H2O.
(6)某学生在关闭活塞x的情况下做此实验时发现,收集到一定体积的气体产物所消耗的甲醇和浓盐酸的混和液的量比正常情况下多(装置的气密性没有问题),其原因是甲醇和盐酸中的氯化氢都是易挥发的物质,在加热时挥发使得一氯甲烷的产率下降
(7)实验结束后,d中收集到的液体中含有一氯甲烷、甲醇、盐酸.
(8)甲醇在一定条件下还可生成二甲醚,二甲醚直接燃料电池具有启动快、效率高等优点,其能量密度高于甲醇(E=5.39kW•h•kg-1)直接燃料电池的能量密度.若电解质为酸性,二甲醚直接燃料电池的理论输出电压为1.20V,能量密度E=8.64kW•h•kg-1
,已知能量密度E=电池输出电能/燃料质量,lkW•h=3.6×l06J,电子电量为1.6×10 -19C,NA为6.02×l023mol-l)
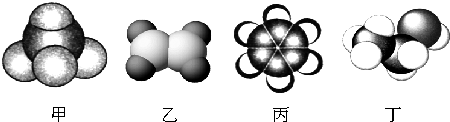
 ;乙的结构式为
;乙的结构式为 ;
;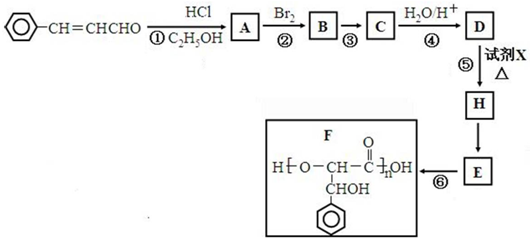
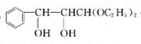 .
. +2Ag(NH3)2OH$\stackrel{△}{→}$
+2Ag(NH3)2OH$\stackrel{△}{→}$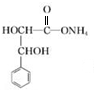 +2Ag↓+3NH3+H2O.
+2Ag↓+3NH3+H2O.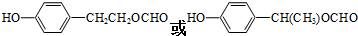 . (任写一种)
. (任写一种)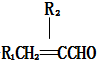
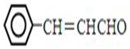 ,设计合成线路(其无机试剂任选),合成线路示意图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=$\stackrel{Br_{2}}{→}$CH2BrH2Br.
,设计合成线路(其无机试剂任选),合成线路示意图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=$\stackrel{Br_{2}}{→}$CH2BrH2Br.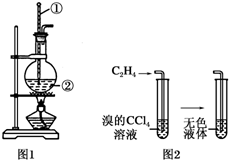 如图是实验室制乙烯的发生装置和乙烯性质实验装置,反应原理为:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2═CH2↑+H2O,回答下列问题:
如图是实验室制乙烯的发生装置和乙烯性质实验装置,反应原理为:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2═CH2↑+H2O,回答下列问题: