题目内容
14.丙烯是一种常见的有机物.下列有关丙烯的化学用语中,不正确的是( )| A. | 实验式 CH2 | B. | 结构简式 CH2=CHCH3 | ||
| C. | 球棍模型 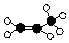 | D. | 聚合后的结构简式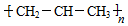 |
分析 A.实验式是指最简式;
B.结构简式是指把分子中各原子连接方式表示出来的式子,通常只适用于以分子形式存在的纯净物;
C.是一种空间填充模型,用来表现化学分子的三维空间分布,在此作图方式中,线代表共价键,可连结以球型表示的原子中心;
D.聚丙烯为碳碳双键相互加成形成的高分子化合物.
解答 解:A.丙烯分子式为C3H6,实验式 CH2 ,故A正确;
B.丙烯含有一个官能团碳碳双键,结构简式为:CH2=CHCH3,故B正确;
C.丙烯为含碳碳双键的烯烃,球棍模型 为: ,故C正确;
,故C正确;
D.聚丙烯为高分子化合物,聚丙烯是由丙烯不饱和的碳原子相互加成得到的,其结构简式为 ,故D错误;
,故D错误;
故选D.
点评 本题考查了化学用语的分析,主要是实验式、结构简式、球棍模型等知识的判断,掌握基础是解题关键,题目难度不大.

练习册系列答案
相关题目
15.下列污水处理的方法中,表示其原理的离子方程式不正确的是( )
| A. | 混凝法,用明矾做混凝剂:Al3++3H2O?Al(OH)3+3H+ | |
| B. | 中和法,用过量CO2中和碱性废水:CO2+2OH-═CO32- | |
| C. | 沉淀法,用Na2S处理含Hg2+废水:Hg2++S2-═HgS↓ | |
| D. | 氧化还原法,用FeSO4将酸性废水中Cr2O72-还原为Cr3+:Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O |
5.下列说法中,正确的是( )
| A. | 氢氧化钠的摩尔质量是40 g | |
| B. | 1 mol硫酸的质量是98g•mol-1 | |
| C. | 甲烷的摩尔质量就是它的相对分子质量 | |
| D. | 17 g NH3含N原子数是6.02×1023个 |
2.表为元素周期表的一部分.
回答下列问题
(1)表中元素原子半径最大的是(写元素符号)Si,Z原子核外电子能量最高的电子亚层是3p.
(2)下列事实能说明Y元素的非金属性比S元素的非金属性强的是ac
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(3)碳酸钠溶液中滴入酚酞,溶液显红色,请用离子方程式解释产生该现象的原因:CO32-+H2O?HCO3-+OH-;在上述红色的溶液中加入少许氯化钙固体,溶液颜色变浅,请用平衡理论解释产生该现象的原因Ca2++CO32-=CaCO3↓,导致溶液中碳酸根离子浓度减少,水解平衡向逆反应方向移动,氢氧根离子浓度减少,碱性减弱.
(4)硫酸工业生产中接触室内发生的反应方程式为2SO2+O2$?_{△}^{催化剂}$2SO3;在实际生产中,操作温度选定400-500℃、压强通常采用常压的原因分别是催化剂在400~500℃时,活性最大,在常压下及400~500℃时,二氧化硫的转化率已经很高,若加压会增加设备、投资和能量消耗.
| 碳 | 氮 | Y | |
| X | 硫 | Z |
(1)表中元素原子半径最大的是(写元素符号)Si,Z原子核外电子能量最高的电子亚层是3p.
(2)下列事实能说明Y元素的非金属性比S元素的非金属性强的是ac
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(3)碳酸钠溶液中滴入酚酞,溶液显红色,请用离子方程式解释产生该现象的原因:CO32-+H2O?HCO3-+OH-;在上述红色的溶液中加入少许氯化钙固体,溶液颜色变浅,请用平衡理论解释产生该现象的原因Ca2++CO32-=CaCO3↓,导致溶液中碳酸根离子浓度减少,水解平衡向逆反应方向移动,氢氧根离子浓度减少,碱性减弱.
(4)硫酸工业生产中接触室内发生的反应方程式为2SO2+O2$?_{△}^{催化剂}$2SO3;在实际生产中,操作温度选定400-500℃、压强通常采用常压的原因分别是催化剂在400~500℃时,活性最大,在常压下及400~500℃时,二氧化硫的转化率已经很高,若加压会增加设备、投资和能量消耗.
9.乙苯( )的二氯代物共有( )
)的二氯代物共有( )
 )的二氯代物共有( )
)的二氯代物共有( )| A. | 15种 | B. | 12种 | C. | 9种 | D. | 6种 |
19.H2S在O2中不完全燃烧生成S和H2O,下列说法中正确的是( )
| A. | 微粒半径:O2->S2- | B. | 还原性:H2S<H2O | ||
| C. | 稳定性:H2S<H2O | D. | 电离方程式:H2S?2H++S2- |
6.下列表示对应化学反应的离子方程式正确的是( )
| A. | 向稀HNO3中滴加Na2SO3溶液:SO32-+2H+═SO2↑+H2O | |
| B. | 向Na2SiO3溶液中通入过量CO2:SiO32-+CO2+H2O═H2SiO3↓+CO32- | |
| C. | 向稀H2SO4中加入过量Ba(OH)2溶液:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O | |
| D. | 向AlCl3溶液中加入过量的NH3•H2O:Al3++4NH3•H2O═AlO2-+4NH4++2H2O |
3.下列离子方程式正确的是( )
| A. | 用FeCl3溶液腐蚀印刷电路板:Fe3++Cu=Fe2++Cu2+ | |
| B. | Na放入水中,产生气体:Na+H2O=Na++OH-+H2↑ | |
| C. | 向FeCl3溶液中滴加淀粉碘化钾溶液,溶液变蓝:2Fe3++2I-=2Fe2++I2 | |
| D. | NaHCO3溶液与NaOH溶液反应:OH-+HCO3-=CO2↑+H2O |
4.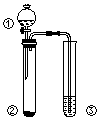 利用如图所示装置进行下列实验,能得出相应实验结论的是( )
利用如图所示装置进行下列实验,能得出相应实验结论的是( )
 利用如图所示装置进行下列实验,能得出相应实验结论的是( )
利用如图所示装置进行下列实验,能得出相应实验结论的是( )| 选项 | ① | ② | ③ | 实验结论 |
| A | 浓盐酸 | Na2CO3 | Na2SiO3溶液 | 非金属性:C>Si |
| B | 食盐水 | 电石 | 溴水 | 乙炔可与溴发生加成反应 |
| C | 浓硝酸 | Fe | NaOH溶液 | 铁和浓硝酸反应可生成NO2 |
| D | 浓硫酸 | Na2SO3 | KMnO4酸性溶液 | SO2具有还原性 |
| A. | A | B. | B | C. | C | D. | D |