题目内容
已知某元素A能与ⅦA族某一元素B生成A本身的最高价化合物,在此化合物中B的含量为92.2%,而在A相应的氧化物AO2中,氧的含量为72.7%.A与B生成的化合物为一无色透明液体,沸点77℃,其蒸气在同温同压下对空气的相对密度为5.31.计算回答下列问题:
(1)计算确定A、B元素名称,并指出A、B元素在周期表中的位置;
(2)写出A元素与B元素形成的化合物及A元素相应的氧化物的分子式和电子式;
(3)指出A与B形成的化合物及A元素相应的氧化物的分子空间构型和分子中的化学键,并列举A与B形成的化合物的两种用途.
(1)计算确定A、B元素名称,并指出A、B元素在周期表中的位置;
(2)写出A元素与B元素形成的化合物及A元素相应的氧化物的分子式和电子式;
(3)指出A与B形成的化合物及A元素相应的氧化物的分子空间构型和分子中的化学键,并列举A与B形成的化合物的两种用途.
分析:A相应的氧化物AO2中,氧的含量为72.7%,则可知
×100%=72.2%,M(A)=12,则A为C元素,某元素A能与ⅦA族某一元素B生成A本身的最高价化合物,A和B形成的化合物为CB4,其蒸气在同温同压下对空气的相对密度为5.31,则12+4×M(B)=29×5.31=154,M(B)=35.5,则B为Cl元素,形成的化合物为CCl4,结合对应的物质以及题目要求解答该题.
| 2×16 |
| 2×16+M(A) |
解答:解:A相应的氧化物AO2中,氧的含量为72.7%,则可知
×100%=72.2%,M(A)=12,则A为C元素,某元素A能与ⅦA族某一元素B生成A本身的最高价化合物,A和B形成的化合物为CB4,其蒸气在同温同压下对空气的相对密度为5.31,则12+4×M(B)=29×5.31=154,M(B)=35.5,则B为Cl元素,形成的化合物为CCl4,
(1)由以上分析可知A为碳元素,位于周期表位于第二周期、ⅣA族,B为氯元素,位于周期表第三周期、ⅦA族,
答:A是碳,位于第二周期、ⅣA,B是氯,位于第三周期、ⅦA;
(2)A元素与B元素形成的化合物的分子式为CCl4,A元素相应的氧化物为CO2,电子式为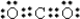 ,
,
答:A元素与B元素形成的化合物的分子式为CCl4,A元素相应的氧化物的电子式为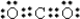 ;
;
(3)A与B形成的化合物为正四面体结构,分子中含有共价键,常用作有机溶剂和灭火剂,
A元素相应的氧化物为直线形分子,含有共价键,
答:CCl4为正四面体,共价键;用途:溶剂、灭火剂.CO2为直线型,共价键.
| 2×16 |
| 2×16+M(A) |
(1)由以上分析可知A为碳元素,位于周期表位于第二周期、ⅣA族,B为氯元素,位于周期表第三周期、ⅦA族,
答:A是碳,位于第二周期、ⅣA,B是氯,位于第三周期、ⅦA;
(2)A元素与B元素形成的化合物的分子式为CCl4,A元素相应的氧化物为CO2,电子式为
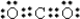 ,
,答:A元素与B元素形成的化合物的分子式为CCl4,A元素相应的氧化物的电子式为
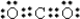 ;
; (3)A与B形成的化合物为正四面体结构,分子中含有共价键,常用作有机溶剂和灭火剂,
A元素相应的氧化物为直线形分子,含有共价键,
答:CCl4为正四面体,共价键;用途:溶剂、灭火剂.CO2为直线型,共价键.
点评:本题考查较为综合,涉及无机物的推断,物质的结构、性质和用途,侧重于学生的基础知识和基本能力的考查,有利于培养学生的科学素养和学习能力,难度不大.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目


 。
。 液: ;
液: ;