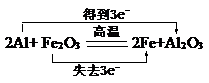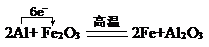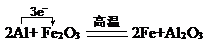题目内容
下列解释过程或事实的方程式不正确的是( )
| A、0.01 mol/L CH3COOH的pH>2:CH3COO-+H2O?CH3COOH+OH- |
| B、用Fecl3溶液腐蚀印刷电路板上的铜:2Fe3++Cu═2Fe2++Cu2+ |
| C、盛装NaOH溶液试剂瓶不能用玻璃塞:2OH-+SiO2═SiO32-+H2O |
| D、自然界各种原生铜的硫化物经氧化、淋滤作用后产生的硫酸铜,遇到难溶的方铅矿(PbS),慢慢转变为铜蓝(CuS):CuSO4+PbS═CuS+PbSO4 |
考点:离子方程式的书写,难溶电解质的溶解平衡及沉淀转化的本质
专题:离子反应专题
分析:A.弱酸属于弱电解质不能完全电离;
B.三价铁离子具有强的氧化性能够氧化铜;
C.氢氧化钠与玻璃中的二氧化硅反应生成具有粘性的硅酸钠;
D.依据沉淀转化的规律解答.
B.三价铁离子具有强的氧化性能够氧化铜;
C.氢氧化钠与玻璃中的二氧化硅反应生成具有粘性的硅酸钠;
D.依据沉淀转化的规律解答.
解答:
解:A.0.01 mol/L CH3COOH的pH>2,是因为:CH3COOH?CH3COO-+H+,故A错误;
B.用Fecl3溶液腐蚀印刷电路板上的铜:2Fe3++Cu═2Fe2++Cu2+,故B正确;
C.盛装NaOH溶液试剂瓶不能用玻璃塞,离子方程式为:2OH-+SiO2═SiO32-+H2O,故C正确;
D.硫化铜沉淀溶解度小于硫化铅,实现沉淀的转化,化学方程式为CuSO4+PbS═CuS+PbSO4,故D正确;
故选:A.
B.用Fecl3溶液腐蚀印刷电路板上的铜:2Fe3++Cu═2Fe2++Cu2+,故B正确;
C.盛装NaOH溶液试剂瓶不能用玻璃塞,离子方程式为:2OH-+SiO2═SiO32-+H2O,故C正确;
D.硫化铜沉淀溶解度小于硫化铅,实现沉淀的转化,化学方程式为CuSO4+PbS═CuS+PbSO4,故D正确;
故选:A.
点评:本题考查了离子方程式的书写,题目难度不大,明确反应的实质是解题关键,注意沉淀能够转化为更难溶的沉淀.

练习册系列答案
相关题目
聚四氟乙烯(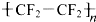 )是不粘锅涂覆物质的主要成分.下列关于聚四氟乙烯的说法,不正确的是( )
)是不粘锅涂覆物质的主要成分.下列关于聚四氟乙烯的说法,不正确的是( )
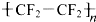 )是不粘锅涂覆物质的主要成分.下列关于聚四氟乙烯的说法,不正确的是( )
)是不粘锅涂覆物质的主要成分.下列关于聚四氟乙烯的说法,不正确的是( )| A、属于高分子化合物 |
| B、单体是CF2=CF2 |
| C、可由加聚反应得到 |
| D、能使高锰酸钾酸性溶液褪色 |
某有机物在氧气里充分燃烧,生成的CO2和H2O的物质的量之比为1:1,由此可以得出该有机物( )
| A、分子中C、H、O的个数比为1:2:3 |
| B、分子中C和H的个数比为1:2 |
| C、分子中肯定不一定含氧原子 |
| D、分子中肯定含有氧原子 |
下列化学式一定表示一种纯净物的是( )
| A、C2H6 |
| B、C2H4Br2 |
| C、C4H10 |
| D、C5H12 |
今年5月7日某公司丢失铱-192放射源的事件再次敲响核安全的警钟.下列关于铱-192(
Ir)的说法正确的是( )
192 77 |
| A、原子序数为77 |
| B、电子数为115 |
| C、中子数为192 |
| D、质量数为77 |
下列说法正确的是( )
| A、500mL 2 mol/L葡萄糖溶液中所含分子数是6.02×1023 |
| B、0.1mol/L Na2CO3溶液中的阴离子总数大于0.1×6.02×1023 |
| C、电解精炼铜时,若阳极质量减少64g,则外电路导线上通过的电子数不一定是2×6.02×1023 |
| D、5.6g铁粉在0.1mol氯气中充分燃烧,转移电子数是0.3×6.02×1023 |
氢气和氟气混合在黑暗处即可发生爆炸而释放出大量的热量.在反应过程中,断裂1molH2中的化学键消耗的能量为Q1kJ,断裂1molF2中的化学键消耗的能量为Q2kJ,形成1molHF中的化学键释放的能量为Q3kJ.下列关系式中正确的是( )
| A、Q1+Q2<2Q3 |
| B、Q1+Q2>2Q3 |
| C、Q1+Q2<Q3 |
| D、Q1+Q2>Q3 |
制备粗硅的反应为:SiO2+2C
Si+2CO↑,其中氧化剂与还原剂的物质的量之比( )
| ||
| A、1:3 | B、3:1 |
| C、1:2 | D、2:1 |