题目内容
燃料电池具有高的发电效率,因而受到重视,可用Li2CO3和Na2CO3的熔融盐混合物做电解质,CO为阴极燃气,空气与CO2的混合气为阳极燃气,制得在650℃下工作的燃料电池,完成有关的电池反应式:阳极反应式:
2CO+2CO32--4e-=4CO2则阳极反应式为 ;总反应式为 .
2CO+2CO32--4e-=4CO2则阳极反应式为
考点:化学电源新型电池
专题:电化学专题
分析:在电解池中,阴极上发生得电子的还原反应,阳极上发生是电子的氧化反应,根据阴阳两极反应可以书写总反应方程式.
解答:
解:在电解池中,阴极上是CO发生失去电子的氧化反应,电极反应为:O2+2CO2+4e-=2CO32-,阳极上是发生失电子的氧化反应,反应式:2CO+2CO32--4e-=4CO2,在转移电子一样多的情况下,两极反应相加得到总反应:2CO+O2=2CO2,
故答案为:O2+2CO2+4e-=2CO32-,2CO+O2=2CO2.
故答案为:O2+2CO2+4e-=2CO32-,2CO+O2=2CO2.
点评:本题考查燃料电池的工作原理以及电极反应式的书写知识,注意知识的迁移和应用是关键,难度不大.

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目
下列实验中,反应速率加快属于由催化剂引起的是( )
| A、电解水时,加少量硫酸可使电解速率加快 |
| B、H2O2中加入少量MnO2,即可迅速放出气体 |
| C、在木炭粉中加入微量氯酸钾,燃烧时极为剧烈 |
| D、用锌与稀硫酸反应制备氢气时,加入少量硫酸铜加快反应 |
已知NA代表阿伏加德罗常数,下列说法正确的是( )
| A、34g H2O2中含有的阴离子数为NA |
| B、标准状况下,22.4L O2作氧化剂时转移电子数一定为4NA |
| C、T℃时,1L pH=6纯水中,含10-6NA个OH- |
| D、10L 0.1mol?L-1的Na2CO3溶液中,Na+、CO32-总数为3NA |
阿伏加德罗常数约为6.02×1023mol-1,下列叙述正确的是( )
| A、2.24L CO2中含有的原子数为0.3×6.02×1023 |
| B、0.1L 3mol?L-1的NH4NO3溶液中含有的NH4+数目为0.3×6.02×1023 |
| C、5.6g铁粉与硝酸反应失去的电子数一定为0.3×6.02×1023 |
| D、1.7g NH3中含有的化学键数目为0.3×6.02×1023 |



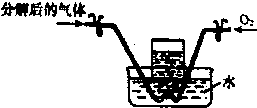 已知Fe(NO3)2受热分解产物为金属氧化物、NO2、O2.某兴趣小组同学对固体产物中Fe的化合物进行了如下探究:
已知Fe(NO3)2受热分解产物为金属氧化物、NO2、O2.某兴趣小组同学对固体产物中Fe的化合物进行了如下探究: