题目内容
分子式为C5H12O且可与金属钠反应放出氢气,且能发生消去反应的有机化合物有(不考虑立体异构)( )
| A、5种 | B、7种 | C、8种 | D、10种 |
考点:同分异构现象和同分异构体
专题:同分异构体的类型及其判定
分析:与金属钠反应放出氢气说明应为醇,先判断醇的同分异构体,然后根据能发生消去反应的醇是与羟基相连碳原子相邻的碳原子上至少有1个氢原子确定;
解答:
解:分子式为C5H12O的有机物,能与金属钠反应放出氢气,说明分子中含有-OH,该物质为戊醇:戊基-C5H11可能的结构有:HOCH2CH2CH2CH2CH3、HOCH(CH3)CH2CH2CH3、HOCH(CH2CH3)2、HOCHCH(CH3)CH2CH3、HOC(CH3)2CH2CH3、HOC(CH3)CH(CH3)2、HOCH2CH2CH(CH3)2、HOCH2C(CH3)3,能发生消去反应的有机化合物有HOCH2CH2CH2CH2CH3、HOCH(CH3)CH2CH2CH3、HOCH(CH2CH3)2、HOCHCH(CH3)CH2CH3、HOC(CH3)2CH2CH3、HOC(CH3)CH(CH3)2、HOCH2CH2CH(CH3)2,共7种;
故选B.
故选B.
点评:本题考查同分异构体的书写,难度较大,注意能发生消去反应的醇是与羟基相连碳原子相邻的碳原子上至少有1个氢原子.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列 电离方程式正确的是( )
| A、NaHS溶于水:NaHS═Na++HS-;HS-+H2O?H3O++S2- |
| B、(NH4)2SO4溶于水:(NH4)2SO4?2NH4++SO42- |
| C、HF溶于水:HF+H2O?F-+2H++OH- |
| D、Al(OH)3的电离:Al(OH)3═Al3++OH- |
下列离子组在指定溶液中能大量共存的是( )
| A、中性溶液:Cu2+、Al3+、NO3-、SO42- | ||
| B、加入苯酚显紫色的溶液:K+、NH4+、Cl-、I- | ||
| C、加入Al能放出大量H2的溶液中:NH4+、Fe2+、NO3-、SO42- | ||
D、常温下,
|
如图,有关铁钉腐蚀(除②外,电解质溶液为食盐水)说法不正确的是( )
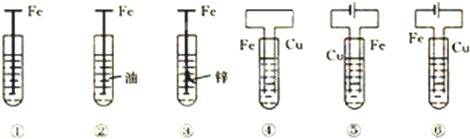

| A、①发生析氢腐蚀 |
| B、③是牺牲阳极的阴极保护法 |
| C、若将⑥的Cu极换成不溶性电极,则⑥是外加电流的阴极保护法 |
| D、腐蚀快到慢的顺序为⑤>④>①>②>③>⑥ |
下列四组物质的分子式或化学式都相同,按物质的分类方法,属于同一类物质的是( )
A、 和CH2-CH-CH2CH2CH2CH3 和CH2-CH-CH2CH2CH2CH3 |
| B、金刚石和石墨 |
| C、CH3-O-CH3和CH3CH2OH |
D、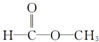 和 和 |
下列说法正确的是( )
| A、甲烷燃烧热的数值为890.3kJ?mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3kJ?mol-1 |
| B、含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则稀醋酸和稀NaOH溶液反应的中和热为57.4kJ/mol |
| C、相同条件下,2mol氢原子所具有的能量小于1mol氢分子所具有的能量 |
| D、同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件的△H相同 |
下列说法正确的是( )
| A、在周期表中,族序数都等于该族元素的最外层电子数 |
| B、碱金属随原子序数的增大,其熔沸点逐渐降低;卤素单质随原子序数的增大,其熔沸点逐渐升高 |
| C、同周期的主族元素从左到右原子半径逐渐减小,它们形成简单的离子半径逐渐增大 |
| D、非金属性最强的元素,其最高价氧化物对应水化物的酸性最强 |