题目内容
某二元酸H2A的电离方程式是:H2A=H++HA-,HA-?A2-+H+.回答下列问题:
(1)Na2A溶液显 (填“酸性”、“碱性”或“中性”),理由是(用离子方程式表示) ;
(2)NaHA溶液显 (填“酸性”、“碱性”或“中性”),理由是(用离子方程式表示) ;
(3)若0.1mol?L-1NaHA溶液的pH=2,则0.1mol?L-1H2A溶液中氢离子的物质的量浓度可能 0.11mol?L-1(填“<”、“>”或“=”),理由
(4)0.1mol?L-1NaHA溶液中各离子浓度由大到小的顺序是 ;
(5)pH=9的Ba(OH)2溶液与pH=12的KOH溶液,按4:1的体积比混合,则混合溶液中H+浓度为 .
(1)Na2A溶液显
(2)NaHA溶液显
(3)若0.1mol?L-1NaHA溶液的pH=2,则0.1mol?L-1H2A溶液中氢离子的物质的量浓度可能
(4)0.1mol?L-1NaHA溶液中各离子浓度由大到小的顺序是
(5)pH=9的Ba(OH)2溶液与pH=12的KOH溶液,按4:1的体积比混合,则混合溶液中H+浓度为
考点:盐类水解的原理,弱电解质在水溶液中的电离平衡
专题:
分析:(1)由HA-?H++A2-可知,Na2A为强碱弱酸盐;
(2)第一步完全电离,第二步部分电离,则Na2A溶液应呈碱性,NaHA溶液中主要存在HA-的电离,则溶液应呈酸性;
(3)0.1mol?L-1H2A溶液,H2A═H++HA-,电离出0.1mol/LH+,0.1mol?L-1NaHA溶液的pH=2,则由HA-?H++A2-可知,电离出0.01mol/LH+,但第一步电离生成的H+抑制了HA-的电离;
(4)NaHA溶液显酸性,存在HA-?H++A2-,则c(Na+)>c(HA-)>c(H+)>c(OH-),结合水的电离分析;
(5)计算出碱溶液混合后的c(OH-),根据Kw=c(OH-)×c(H+)=10-14,可计算出c(H+).
(2)第一步完全电离,第二步部分电离,则Na2A溶液应呈碱性,NaHA溶液中主要存在HA-的电离,则溶液应呈酸性;
(3)0.1mol?L-1H2A溶液,H2A═H++HA-,电离出0.1mol/LH+,0.1mol?L-1NaHA溶液的pH=2,则由HA-?H++A2-可知,电离出0.01mol/LH+,但第一步电离生成的H+抑制了HA-的电离;
(4)NaHA溶液显酸性,存在HA-?H++A2-,则c(Na+)>c(HA-)>c(H+)>c(OH-),结合水的电离分析;
(5)计算出碱溶液混合后的c(OH-),根据Kw=c(OH-)×c(H+)=10-14,可计算出c(H+).
解答:
解:(1)由HA-?H++A2-可知,Na2A为强碱弱酸盐,A2-水解显碱性,水解离子反应为A2-+H2O?HA-+OH-,故答案为:碱性;A2-+H2O?HA-+OH-;
(2)第一步完全电离,则NaHA溶液中主要存在HA-的电离,发生HA-?A2-+H+,溶液呈酸性,故答案为:酸性;HA-?A2-+H+;
(3)0.1mol?L-1H2A溶液,H2A═H++HA-,电离出0.1mol/LH+,0.1mol?L-1NaHA溶液的pH=2,则由HA-?H++A2-可知,电离出0.01mol/LH+,但第一步电离生成的H+抑制了HA-的电离,所以溶液中氢离子的物质的量浓度小于0.1mol/L+0.01mol/L=.11mol?L-1,
故答案为:<;H2A电离产生的H+抑制了HA-的电离;
(4)NaHA溶液显酸性,存在HA-?H++A2-,则c(Na+)>c(HA-)>c(H+)>c(OH-),结合水的电离H2O?H++OH-,则c(H+)>c(A2-),即NaHA溶液中各种离子浓度由大到小的顺序为c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-),
故答案为:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-);
(5)pH=9的Ba(OH)2溶液中c(OH-)=10-5mol/L,pH=12的KOH溶液中c(OH-)=10-2mol/L,
按4:1的体积比混合,c(OH-)=
mol/L≈0.2×10-2mol/L,
则c(H+)=
=5×10-12mol/L,
故答案为:5×10-12mol/L.
(2)第一步完全电离,则NaHA溶液中主要存在HA-的电离,发生HA-?A2-+H+,溶液呈酸性,故答案为:酸性;HA-?A2-+H+;
(3)0.1mol?L-1H2A溶液,H2A═H++HA-,电离出0.1mol/LH+,0.1mol?L-1NaHA溶液的pH=2,则由HA-?H++A2-可知,电离出0.01mol/LH+,但第一步电离生成的H+抑制了HA-的电离,所以溶液中氢离子的物质的量浓度小于0.1mol/L+0.01mol/L=.11mol?L-1,
故答案为:<;H2A电离产生的H+抑制了HA-的电离;
(4)NaHA溶液显酸性,存在HA-?H++A2-,则c(Na+)>c(HA-)>c(H+)>c(OH-),结合水的电离H2O?H++OH-,则c(H+)>c(A2-),即NaHA溶液中各种离子浓度由大到小的顺序为c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-),
故答案为:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-);
(5)pH=9的Ba(OH)2溶液中c(OH-)=10-5mol/L,pH=12的KOH溶液中c(OH-)=10-2mol/L,
按4:1的体积比混合,c(OH-)=
| 4×10-5+10-2 |
| 5 |
则c(H+)=
| 1×10-14 |
| 0.2×10-2 |
故答案为:5×10-12mol/L.
点评:本题考查盐类水解,明确习题中的信息是解答本题的关键,注意二元酸的两步电离特点,题目难度中等.

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目
下列有关生活常识的说法中,正确的是( )
| A、用完后的废电池应该集中回收处理 |
| B、天然果汁中不含任何化学物质 |
| C、“绿色食品”指颜色为绿色的食品 |
| D、“白色污染”是白色粉尘造成的污染 |
向Na2CO3溶液中滴入2滴酚酞试液,溶液呈浅红色,微热后溶液的颜色将( )
| A、变深 | B、变浅 | C、不变 | D、褪去 |
葡萄糖的结构简式为CH2OH-CHOH-CHOH-CHOH-CHOH-CHO,下列关于葡萄糖的说法错误的是( )
| A、葡萄糖是单糖 |
| B、含有5个羟基(-OH) |
| C、含有1个醛基(-CHO) |
| D、含有1个羧基(-COOH) |
下列对进行焰色反应的实验操作注意事项的说明,正确的是( )
①钾的火焰颜色要透过蓝色钴玻璃观察
②先灼烧铂丝到火焰呈原色时,再蘸被检验物质
③每次实验后都要将铂丝蘸稀硫酸后灼烧至火焰呈无色为止
④没有铂丝可用无锈铁丝代替.
①钾的火焰颜色要透过蓝色钴玻璃观察
②先灼烧铂丝到火焰呈原色时,再蘸被检验物质
③每次实验后都要将铂丝蘸稀硫酸后灼烧至火焰呈无色为止
④没有铂丝可用无锈铁丝代替.
| A、仅③不正确 |
| B、仅④不正确 |
| C、③④不正确 |
| D、②③④不正确 |
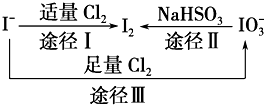 碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种微粒之间有如图所示关系(已知:NaHSO3做还原剂,被氧化为Na2SO4),根据图示转化关系推测下列说法不正确的是( )
碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种微粒之间有如图所示关系(已知:NaHSO3做还原剂,被氧化为Na2SO4),根据图示转化关系推测下列说法不正确的是( )| A、海带中提取碘过程中,将I-氧化成I2所通入的Cl2不宜过量 |
| B、足量Cl2能使湿润的KI淀粉试纸先变蓝后变白的原因可能是:5Cl2+I2+6H2O═2HIO3+10HCl |
| C、由图可知氧化性的强弱顺序为Cl2>I2>IO3- |
| D、途径Ⅱ中若生成1 mol I2,反应中转移的电子数为10NA |