题目内容
13.下列说法中正确的是( )| A. | 乙烷和乙烯均可使酸性KMnO4溶液褪色 | |
| B. | 甲烷燃烧会生成CO2,因此不属于清洁能源 | |
| C. | 向甲苯中滴入少量浓溴水,振荡,静置,溶液分层,上层呈橙红色,下层几乎无色,可知甲苯和溴水发生取代反应,使溴水褪色 | |
| D. | 水煤气、裂解气、焦炉气、天然气都是混合物 |
分析 A.乙烷和高锰酸钾不反应;
B.甲烷完全燃烧不生成有害气体;
C.甲苯和溴水不反应;
D.水煤气是CO和H2的混合物;裂解气是乙烯、丙烯等混合物;焦炉气是混合物,其主要成分为氢气(55%~60%)和甲烷(23%~27%),另外还含有少量的一氧化碳(5%~8%),是混合物;天然气主要成分是甲烷.
解答 解:A.乙烯含有碳碳双键,可与高锰酸钾发生氧化还原反应,乙烷和高锰酸钾不反应,故A错误;
B.甲烷完全燃烧不生成有害气体,属于清洁能源,故B错误;
C.甲苯和溴水不反应,可与液溴在催化作用下发生取代反应,故C错误;
D.水煤气是CO和H2的混合物;裂解气是乙烯、丙烯等混合物;焦炉气是混合物,其主要成分为氢气(55%~60%)和甲烷(23%~27%),另外还含有少量的一氧化碳(5%~8%),是混合物;天然气主要成分是甲烷,还还有其他杂质,故D正确;
故选D.
点评 本题考查有机物的结构和性质,为高考常见题型,侧重于学生的分析能力的考查,注意把握有机物的结构和官能团的性质,为解答该类题目的关键,难度不大.

练习册系列答案
相关题目
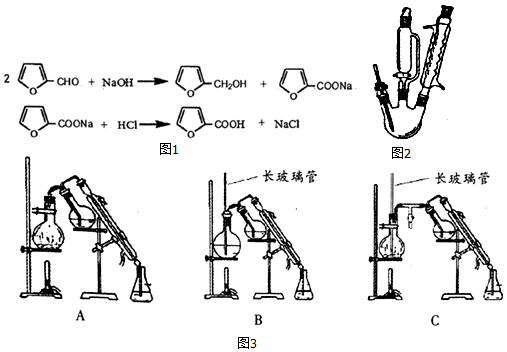
4.糠酸又称呋喃甲酸,在食品工业作防腐剂,还可用于合成树脂或医药、香料等的中 间体.以米槺或玉米芯提取的呋喃甲醛为原料合成糠酸反应如图1
几种有机物性质如表:
刚果红试纸pH变色范围:3.0(蓝紫色)~5.0(红色)
呋喃甲酸的实验室制备方法如图2:
三颈瓶中放人3.28mL(0.04mol)新蒸呋喃甲醛,控温8~12℃下滴加4mL40%NaOH溶液,并
磁力搅拌回流30分钟.向反应混合物滴加蒸馏水(约15mL)使其恰好澄清,用50mL乙醚萃取分液,其水溶液用水蒸气蒸馏,弃去镏出物,慢慢滴加2:1盐酸到pH=3,搅拌,析出结晶,抽滤并用少量水洗涤抽干,得精产品1.5g.
回答以下问题:
(1)三颈瓶中反应需要搅拌回流30分钟的原因是呋喃甲醛微溶于水,搅拌充分混合加快反应速率.
(2)呋喃甲醛在碱中反应大量放热,实验中需要控温8-12℃,其操作方法冷水浴.
(3)50mL乙醚萃取分液,除去呋喃甲醇的操作方法是C.
A、直接用50mL乙醚萃取分液
B、将溶液分两份,乙醚也分两份,分别萃取,萃取液合并
C、先用30mL乙醚萃取分液,再分别州l0mL乙醚萃取两次,并将三次萃取液合并
(4)乙醚提取后的水溶液要用盐酸酸化.配制100mL 2:1稀盐酸(水与盐酸体积比)的方法是用量筒分别量取66ml水、34ml浓盐酸,于烧杯中混合,用玻璃棒搅拌均匀;判断盐酸加入足量的方法是使用刚果红试纸测定溶液pH,当试纸变蓝紫色时,说明加入盐酸足量 (上层清液中继续滴加盐酸,不产生浑浊,说明盐酸加入足量).
(5)乙醚易挥发、易燃,蒸气可使人失去知觉,在蒸馏回收乙醚时注意:在水浴上进行蒸馏,切忌直接明火加热;水蒸气蒸馏的方法应选择(图3)C(填字母序号);
(6)计算呋喃甲酸的产率67%.
几种有机物性质如表:
| 名称 | 性状 | 相对分 子质量 | 溶解度 | |||
| 冷水 | 热水 | 乙醇 | 乙醚 | |||
| 呋喃甲醛 | 无色液体 | 96 | 微溶 | 易溶 | 易溶 | 互溶 |
| 呋喃甲醇 | 无色液体 | 98 | 互溶 | 互溶 | 易溶 | 易溶 |
| 呋喃甲酸 | 无色晶体 | 112 | 微溶 | 易溶 | 可溶 | 易溶 |
呋喃甲酸的实验室制备方法如图2:
三颈瓶中放人3.28mL(0.04mol)新蒸呋喃甲醛,控温8~12℃下滴加4mL40%NaOH溶液,并
磁力搅拌回流30分钟.向反应混合物滴加蒸馏水(约15mL)使其恰好澄清,用50mL乙醚萃取分液,其水溶液用水蒸气蒸馏,弃去镏出物,慢慢滴加2:1盐酸到pH=3,搅拌,析出结晶,抽滤并用少量水洗涤抽干,得精产品1.5g.
回答以下问题:
(1)三颈瓶中反应需要搅拌回流30分钟的原因是呋喃甲醛微溶于水,搅拌充分混合加快反应速率.
(2)呋喃甲醛在碱中反应大量放热,实验中需要控温8-12℃,其操作方法冷水浴.
(3)50mL乙醚萃取分液,除去呋喃甲醇的操作方法是C.
A、直接用50mL乙醚萃取分液
B、将溶液分两份,乙醚也分两份,分别萃取,萃取液合并
C、先用30mL乙醚萃取分液,再分别州l0mL乙醚萃取两次,并将三次萃取液合并
(4)乙醚提取后的水溶液要用盐酸酸化.配制100mL 2:1稀盐酸(水与盐酸体积比)的方法是用量筒分别量取66ml水、34ml浓盐酸,于烧杯中混合,用玻璃棒搅拌均匀;判断盐酸加入足量的方法是使用刚果红试纸测定溶液pH,当试纸变蓝紫色时,说明加入盐酸足量 (上层清液中继续滴加盐酸,不产生浑浊,说明盐酸加入足量).
(5)乙醚易挥发、易燃,蒸气可使人失去知觉,在蒸馏回收乙醚时注意:在水浴上进行蒸馏,切忌直接明火加热;水蒸气蒸馏的方法应选择(图3)C(填字母序号);
(6)计算呋喃甲酸的产率67%.

5.下列图示实验正确的是( )
| A. |  将海带灼烧灰化 | B. | 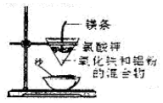 铝热反应 | ||
| C. | 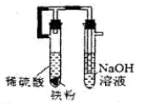 制取氢氧化亚铁 | D. | 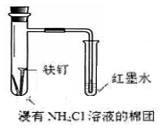 验证铁的吸氧腐蚀 |
8.将17克气体H2A通入水中形成500ml溶液,完全中和该二元酸用去NaOH 40克,则 下列说法正确的是( )
| A. | 该气体的摩尔质量为34 | B. | 500ml溶液物质的量浓度为2mol/L | ||
| C. | 标况下该气体的摩尔体积为22.4 L | D. | 17克该气体物质的量为0.5mol |
18.下列叙述错误的是( )
| A. | 10mL质量分数为98%的H2SO4,用10mL水稀释后,H2SO4的质量分数大于49% | |
| B. | 地球上99%的溴蕴藏在大海中,故溴被称为“海洋元素” | |
| C. | 在标况下,将22.4L氨气溶于1L水中,得到1mol/L的氨水 | |
| D. | 向两等份不饱和的烧碱溶液中分别加入一定量的Na2O2和Na2O,使溶液均恰好饱和,则加入的Na2O2与Na2O的物质的量之比等于1:1(保持温度不变) |
2.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,33.6 L氟化氢中含有氟原子的数目为1.5NA | |
| B. | 5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2↑+9H2O反应中,生成28 g N2时,转移的电子数目为3.75NA | |
| C. | 50 mL 18.4 mol•L-1浓硫酸与足量铜加热反应,生成SO2分子的数目为0.46NA | |
| D. | 将含有0.1 mol FeCl3的饱和溶液滴入沸水中,生成的胶体中含胶体粒子的数目为0.1NA |
3.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 6.4gO2和O3的混合气体,含氧原子数为0.4NA | |
| B. | 分子标准状况下,11.2LCCl4中含分子数为0.5NA | |
| C. | 1mol乙酸(忽视挥发损失)与足量的C2H518OH在浓硫酸作用下加热,充分反应可生成NA个CH3CO18OC2H5 | |
| D. | 常温常压下,7.8gNa2O2含离子数为0.4NA |
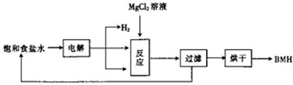 BMH{碱式次氯酸镁}[Mg2ClO(OH)n•H2O]}是一种白色粉末.难溶于水,是常用的无机抗菌剂,其一种生产工艺如图所示.
BMH{碱式次氯酸镁}[Mg2ClO(OH)n•H2O]}是一种白色粉末.难溶于水,是常用的无机抗菌剂,其一种生产工艺如图所示.