题目内容
15.碳在氧气或臭氧中燃烧的能量变化如图.下列说法不正确的是( )
| A. | 3O2(g)=2O3(g)△H=+242.4kJ•mol-1 | |
| B. | 氧气比臭氧稳定,大气中臭氧层易被破坏 | |
| C. | 断裂l mol O2(g)中的共价键吸收的能量比形成1 molCO2(g)中的共价键放出的能量少 | |
| D. | 相同物质的量的氧气比臭氧所含的能量高 |
分析 由能量变化图可知①C(s)+O2(g)=CO2(g)△H=-393.5kJ•mol-1,②C(s)+$\frac{2}{3}$O3(g)=CO2(g)△H=-474.3kJ•mol-1,由盖斯定律将①×3-②×3可得③3O2(g)=2O3(g)△H=+242.4kJ•mol-1,以此解答该题.
解答 解:A.由以上分析可知3O2(g)=2O3(g)△H=+242.4kJ•mol-1,故A正确;
B.由A可知O2的能量比O3低,物质的能量越低越稳定,故B正确;
C.由C(s)+O2(g)=CO2(g)△H=-393.5kJ•mol-1可知,断裂l mol O2(g)中的共价键吸收的能量比形成1 molCO2(g)中的共价键放出的能量少,故C正确;
D.由3O2(g)=2O3(g)△H=+242.4kJ•mol-1,可知相同物质的量的氧气比臭氧所含的能量低,故D错误.
故选D.
点评 本题考查反应热与焓变,侧重于学生的分析能力和计算能力的考查,为高考常见题型和高频考点,注意把握图象,根据图象书写热化学方程式,为解答该题的关键,难度中等.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
5.下列反应不能用离子方程式“H++OH-=H2O”表示的是( )
| A. | H2SO4溶液与NaOH溶液混合 | B. | HCl气体通入Ca(OH)2溶液中 | ||
| C. | HNO3溶液与KOH溶液混合 | D. | NH4HSO4溶液与NaOH溶液混合 |
6.下列各组离子一定能大量共存的是( )
| A. | 在强碱溶液中:Na+、K+、CO32-、NO3- | |
| B. | 在pOH=2的溶液中:NH4+、Na+、SO42-、AlO2- | |
| C. | 在pH=1的溶液中:K+、Ag+、Mg2+、Fe2+ | |
| D. | 水电离出来的c(H+)=1×10-13 mol•L-1的溶液:K+、HCO3-、Br-、Ba2+ |
7.下列分散系中分散质粒子最小的是( )
| A. | 葡萄糖溶液 | B. | Fe(OH)3胶体 | ||
| C. | 少量植物油和水混合 | D. | 泥水 |
4.有X、Y、Z、W、M五种原子序数增大的短周期元素,其中X、M同主族; Z+与Y2-具有相同的电子层结构,W是地壳中含量最多的金属,X与W的原子序数之和等于Y与Z的原子序数之和;下列序数不正确的是( )
| A. | X有多种同素异形体,而Y不存在同素异形体 | |
| B. | X、M均能与氯形成由极性键构成的XCl4、MCl4分子 | |
| C. | W的氧化物对应的水化物可与Z的最高价氧化物对应的水化物反应 | |
| D. | 离子半径大小:r(Y2-)>r(W3+) |
5.pH=1的无色溶液中,下列离子一定能大量共存的是( )
| A. | NH4+、Ag+、PO43-、Cl- | B. | Al3+、H+、I-、HCO3- | ||
| C. | K+、Na+、NO3-、MnO4- | D. | Al3+、Mg2+、SO42-、NO3- |
 现有部分元素的存在,性质和原子结构如下所述:
现有部分元素的存在,性质和原子结构如下所述: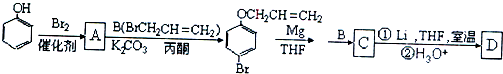
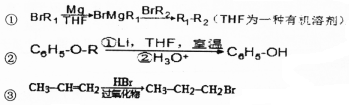
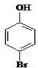 、
、 .
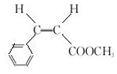
. 是化合物B的一种同分异构体,用1H核磁共振谱可以证明该化合物中有2种氢处于不同的化学环境.
是化合物B的一种同分异构体,用1H核磁共振谱可以证明该化合物中有2种氢处于不同的化学环境. 的有机反应类型取代反应.
的有机反应类型取代反应. .
.
 .
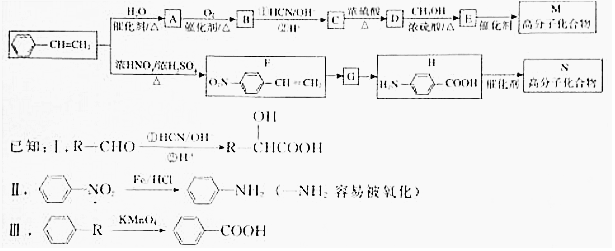
.
 .
. 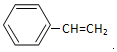 →F的反应类型为取代 反应.
→F的反应类型为取代 反应.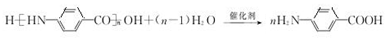 .
. .
. .
.