题目内容
在一个容积为V L的密闭容器中,放入2 L A(g)和1 L B(g),在一定条件下发生下列反应:3A(g)+B(g)?nC(g)+2D(g).达到平衡后,A物质的量浓度减小
,混合气的平均摩尔质量增大
,则该反应的化学方程式中n的值是多少?
| 1 |
| 2 |
| 1 |
| 8 |
考点:化学平衡的计算
专题:化学平衡专题
分析:3A(g)十B(g)?nC(g)+2D(g)达到平衡后,混合气体的平均摩尔质量增大,则该反应为气体体积缩小的反应,结合氧气变化的特征和其他物质的量关系分析,以此来解答.
解答:
解:在一个容积为VL的密闭容器中放入2LA(g)和1L B(g),在一定条件下发生下列反应:3A(g)十B(g)?nC(g)+2D(g),
达到平衡后,混合气体的平均摩尔质量增大,由M=
可知,
A、B、C、D均为气体,由质量守恒定律可知,气体的总质量不变,
则该反应为气体体积缩小的反应,
即3+1>n+2,
所以n<2,化学计量数为整数,所以n=1;
答:该反应的化学方程式中n的值是1;
达到平衡后,混合气体的平均摩尔质量增大,由M=
| m |
| n |
A、B、C、D均为气体,由质量守恒定律可知,气体的总质量不变,
则该反应为气体体积缩小的反应,
即3+1>n+2,
所以n<2,化学计量数为整数,所以n=1;
答:该反应的化学方程式中n的值是1;
点评:本题考查化学平衡的计算,明确混合气体平均摩尔质量增大得出该反应为气体体积缩小的反应为解答本题的关键,不必要进行具体的计算,题目难度不大.

练习册系列答案
相关题目
某化学反应经过2min,生成物Y的浓度从0增加到0.24mol/L,而反应物X的浓度从0.3mol/L变成0.22mol/L.该反应可能是( )
| A、X+2Z→3Y |
| B、X+Z→2Y |
| C、3X→Y+Z |
| D、X→Y+3Z |
在一密闭容器中,用等物质的量的A和B发生如下反应:A(气)+2B(气)?2C(气)反应到5min 时,A的转化率为0.4.则此时混合物中物质的量n(A)、n(B)和n(C)应满足的关系是( )
| A、n(A)=n(C) |
| B、n(B)=n(C) |
| C、n(A)+n(B)=n(C) |
| D、n(B)+n(C)=n(A) |
N2和H2的物质的量之比为2:3的混合气体充入一容积固定的密闭容器中,在一定的条件下发生反应,当达到平衡时,容器内的压强为反应开始时的
,则N2的转化率为( )
| 4 |
| 5 |
| A、50% | B、37.5% |
| C、25% | D、12.5% |
下列有机物的命名不正确的是( )
| A、HCHO 蚁醛 |
| B、C6H5OH 苯酚 |
| C、CH3Cl 1-氯甲烷 |
D、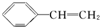 苯乙烯 苯乙烯 |
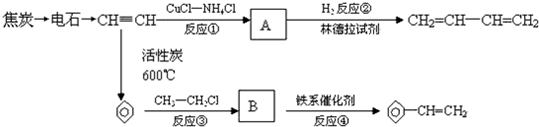
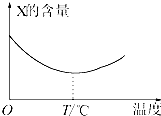 两种气态单质X和Y能直接化合生成Z(可逆反应),如将X和Y按一定比例混合并压入密闭容器中,在不同温度下经过一段时间后,反应混合物中X的含量变化如图所示,回答下列问题:
两种气态单质X和Y能直接化合生成Z(可逆反应),如将X和Y按一定比例混合并压入密闭容器中,在不同温度下经过一段时间后,反应混合物中X的含量变化如图所示,回答下列问题: 某种食品的配料标签如图所示.
某种食品的配料标签如图所示.