题目内容
在新材料领域,碳族元素有许多应用,请用所学相关知识回答下列问题:
(1)碳纳米管由单层或多层石墨层卷曲而成,其结构类似于石墨晶体,每个碳原子通过 杂化与周围碳原子成键,多层碳纳米管的层与层之间靠 结合在一起.
(2)CH4中共用电子对偏向C,SiH4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为 .CH4的熔点比SiH4(填“高”或“低”) ,原因是 .
(3)用价层电子对互斥理论推断SnBr2分子中Sn-Br键的键角 120°(填“>”、“<”或“=”),原因是 .
(4)铅、钡、氧形成的某化合物的晶胞结构是:Pb4+处于立方晶胞顶点,Ba2+处于晶胞中心,O2-处于晶胞棱边中心.该化合物化学式为 ,每个Ba2+与 个O2-配位.
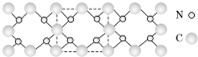
(5)氮化碳结构如图,其中β氮化碳硬度超过金刚石晶体,成为首屈一指的超硬新材料.在氮化碳晶体中每个碳原子与 个氮原子相连,每个氮原子与 个碳原子相连,化学式为 .
(1)碳纳米管由单层或多层石墨层卷曲而成,其结构类似于石墨晶体,每个碳原子通过
(2)CH4中共用电子对偏向C,SiH4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为
(3)用价层电子对互斥理论推断SnBr2分子中Sn-Br键的键角
(4)铅、钡、氧形成的某化合物的晶胞结构是:Pb4+处于立方晶胞顶点,Ba2+处于晶胞中心,O2-处于晶胞棱边中心.该化合物化学式为
(5)氮化碳结构如图,其中β氮化碳硬度超过金刚石晶体,成为首屈一指的超硬新材料.在氮化碳晶体中每个碳原子与

考点:晶胞的计算,元素电离能、电负性的含义及应用,键能、键长、键角及其应用,不同晶体的结构微粒及微粒间作用力的区别
专题:化学键与晶体结构
分析:(1)石墨是层状结构,每层中每个C原子与周围的3个C原子成σ键,键角为120°(这些都是实验数据得出的),根据价层电子对互斥理论分析,层层之间存在分子间作用力;
(2)分子中共用电子对偏向于电负性大的原子,偏离于电负性小的原子;分子晶体中,氢化物的熔沸点与其相对分子质量成正比;
(3)中心原子的孤电子对对成键电子对有排斥作用;
(4)利用均摊法确定其化学式;
(5)根据氮化碳结构知,在氮化碳晶体中每个碳原子与4个氮原子相连,每个氮原子与3个碳原子相连,据此判断其化学式.
(2)分子中共用电子对偏向于电负性大的原子,偏离于电负性小的原子;分子晶体中,氢化物的熔沸点与其相对分子质量成正比;
(3)中心原子的孤电子对对成键电子对有排斥作用;
(4)利用均摊法确定其化学式;
(5)根据氮化碳结构知,在氮化碳晶体中每个碳原子与4个氮原子相连,每个氮原子与3个碳原子相连,据此判断其化学式.
解答:
解:(1)石墨是层状结构,每层中每个C原子与周围的3个C原子成σ键,且含有一个π键,所以C原子杂化方式为sp2,键角为120°,层层之间存在分子间作用力,
故答案为:sp2;分子间作用力(或范德华力);
(2)元素的电负性越大,其吸引电子能力越大,根据元素吸引电子能力知,这三种元素电负性大小顺序是C>H>Si,硅烷和甲烷都是分子晶体,硅烷相对分子质量大于甲烷,二者结构和组成相似,所以甲烷的范德华力吸引硅烷,则CH4的熔点比SiH4低,
故答案为:C>H>Si;低;两分子结构与组成相似,CH4的相对分子量小,范德华力小;
(3)SnBr2分子中Sn原子价层电子对个数=2+
×(4-2×1)=3且含有一个孤电子对,所以该分子为V形分子,孤电子对对成键电子对有排斥作用,所以其键角小于120°,
故答案为:<;中心原子的孤电子对对成键电子对有排斥作用;
(4)Pb4+处于立方晶胞顶点,Ba2+处于晶胞中心,O2-处于晶胞棱边中心,则该晶胞中Pb4+个数=8×
=1,Ba2+个数为1,O2-个数=12×
=3,所以其化学式为BaPbO3,每个Ba2+与12个O2-配位,
故答案为:BaPbO3;12;
(5)根据氮化碳结构知,在氮化碳晶体中每个碳原子与4个氮原子相连,每个氮原子与3个碳原子相连,则C原子和N原子个数之比为3:4,所以其化学式为C3N4,
故答案为:4;3;C3N4.
故答案为:sp2;分子间作用力(或范德华力);
(2)元素的电负性越大,其吸引电子能力越大,根据元素吸引电子能力知,这三种元素电负性大小顺序是C>H>Si,硅烷和甲烷都是分子晶体,硅烷相对分子质量大于甲烷,二者结构和组成相似,所以甲烷的范德华力吸引硅烷,则CH4的熔点比SiH4低,
故答案为:C>H>Si;低;两分子结构与组成相似,CH4的相对分子量小,范德华力小;
(3)SnBr2分子中Sn原子价层电子对个数=2+
| 1 |
| 2 |
故答案为:<;中心原子的孤电子对对成键电子对有排斥作用;
(4)Pb4+处于立方晶胞顶点,Ba2+处于晶胞中心,O2-处于晶胞棱边中心,则该晶胞中Pb4+个数=8×
| 1 |
| 8 |
| 1 |
| 4 |
故答案为:BaPbO3;12;
(5)根据氮化碳结构知,在氮化碳晶体中每个碳原子与4个氮原子相连,每个氮原子与3个碳原子相连,则C原子和N原子个数之比为3:4,所以其化学式为C3N4,
故答案为:4;3;C3N4.
点评:本题考查物质结构和性质,涉及晶胞计算、电负性、键角等知识点,利用均摊法、元素周期律、价层电子对互斥理论等知识点分析解答,难点是价层电子对个数的计算、晶胞的计算,同时考查学生空间想象能力,题目难度中等.

练习册系列答案
 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
氧离子的结构示意图是( )
A、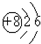 |
B、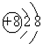 |
C、 |
D、 |
下列有关摩尔使用的说法中不正确的是( )
| A、1摩尔氧原子 |
| B、1摩尔氧分子 |
| C、1摩尔氧气 |
| D、1摩尔氧 |
互为同素异形体的一组物质是( )
| A、16 8O和18 8O |
| B、O2和O3 |
| C、CH≡CH和CH2=CH2 |
D、CH3CH2CH2CH3和 |
欲鉴别碳酸钠和亚硫酸钠,应选用的试剂是( )
| A、氯化钡溶液 |
| B、盐酸和品红溶液 |
| C、盐酸和澄清石灰水 |
| D、氯化钡溶液和盐酸 |
今有含碳酸氢钠的碳酸钠样品10.0g,放在空气中加热至质量恒重为9.38g;则样品中碳酸钠的质量分数为( )
| A、91.6% |
| B、83.2% |
| C、75.0% |
| D、67.6% |
NO与NO2的混合气体60ml,通入水中,最后收集到的气体体积为40ml(气体体积均在相同条件下测定),则原混合气体中NO与NO2的体积比为( )
| A、1:2 | B、2:3 |
| C、3:2 | D、1:1 |
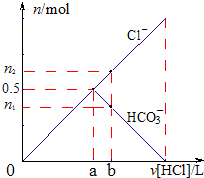 向某碳酸钠溶液中逐滴加1mol?L─1的盐酸,测得溶液中Cl-、HCO3-的物质的量随加入盐酸体积的关系如图所示,其中n2:n1=3:2
向某碳酸钠溶液中逐滴加1mol?L─1的盐酸,测得溶液中Cl-、HCO3-的物质的量随加入盐酸体积的关系如图所示,其中n2:n1=3:2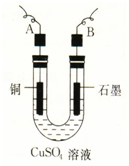 某学生用电解纯净的CuSO4溶液的方法,并根据电极上析出Cu的质量(m g)以及电极上产生气体的体积(V mL 标准状况)来测定Cu的相对原子质量,所用部分仪器及装置如图所示,回答下列问题:
某学生用电解纯净的CuSO4溶液的方法,并根据电极上析出Cu的质量(m g)以及电极上产生气体的体积(V mL 标准状况)来测定Cu的相对原子质量,所用部分仪器及装置如图所示,回答下列问题: