题目内容
模拟铁的电化学防护的实验装置如图所示,下列说法不正确的是( )
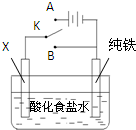

| A、若X为碳棒,开关K须置于A处才可以减缓铁的腐蚀 | B、若X为锌棒,开关K须置于B处才可以减缓铁的腐蚀 | C、若X为铜棒,开关K须置于A处才可以减缓铁的腐蚀 | D、若X为碳棒,开关K置于A、B之间(如图)时,向溶液中滴加K3[Fe(CN)6]溶液,出现蓝色沉淀 |
分析:开关置于A处,该装置是电解池,X作阳极,铁作阴极,阳极上失电子发生氧化反应,阴极上得电子发生还原反应;
开关置于B处,该装置是原电池,较活泼的金属铁作负极,负极上失电子发生氧化反应,正极上得电子发生还原反应.根据金属的防护,若K置于A处,形成电解池,必须让被保护的金属接电源负极;若开关K置于B处,形成原电池,铁作负极,发生吸氧腐蚀,金属被腐蚀.
开关置于B处,该装置是原电池,较活泼的金属铁作负极,负极上失电子发生氧化反应,正极上得电子发生还原反应.根据金属的防护,若K置于A处,形成电解池,必须让被保护的金属接电源负极;若开关K置于B处,形成原电池,铁作负极,发生吸氧腐蚀,金属被腐蚀.
解答:解:A.若X为碳棒,开关K置于A处,该装置是电解池,铁作阴极而被保护,所以可以减缓铁的腐蚀,故A正确;
B.若X为锌棒,开关K置于A处,铁棒作阴极而被保护,开关置于B处,铁作正极而被保护,所以均可减缓铁的腐蚀,故B错误;
C.若X为铜棒,开关K置于A处时,该装置是电解池,铁作阴极,被保护,可以减缓铁的腐蚀,故C正确;
D.若X为碳棒,开关K置于A、B之间(如图)时,金属铁会被腐蚀,生成亚铁离子,含Fe2+的溶液与铁氰化钾K3[Fe(CN)6]溶液反应生成具有特征蓝色的铁氰化亚铁沉淀,故D正确;
故选B.
B.若X为锌棒,开关K置于A处,铁棒作阴极而被保护,开关置于B处,铁作正极而被保护,所以均可减缓铁的腐蚀,故B错误;
C.若X为铜棒,开关K置于A处时,该装置是电解池,铁作阴极,被保护,可以减缓铁的腐蚀,故C正确;
D.若X为碳棒,开关K置于A、B之间(如图)时,金属铁会被腐蚀,生成亚铁离子,含Fe2+的溶液与铁氰化钾K3[Fe(CN)6]溶液反应生成具有特征蓝色的铁氰化亚铁沉淀,故D正确;
故选B.
点评:本题考查原电池和电解池原理,明确电极上得失电子是解本题关键,电极反应式的书写是学习难点,同时也是考试热点,应重点掌握.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
 (2012?南宁一模)模拟铁的电化学防护的实验装置如图所示,下列说法错误的是( )
(2012?南宁一模)模拟铁的电化学防护的实验装置如图所示,下列说法错误的是( )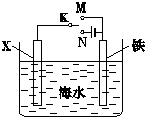 (1)利用如图装置,可以模拟铁的电化学防护.若X为碳棒,为减缓铁的腐蚀,开关K应该置于
(1)利用如图装置,可以模拟铁的电化学防护.若X为碳棒,为减缓铁的腐蚀,开关K应该置于
