题目内容
(1)写出表示含有8个质子、10个中子、10个电子的离子的符号 (写成
Xn-的形式).
(2)周期表中位于第8纵行的铁元素属于第 族.
(3)周期表中最活泼的非金属元素位于第 纵行 族.
A Z |
(2)周期表中位于第8纵行的铁元素属于第
(3)周期表中最活泼的非金属元素位于第
考点:元素周期表的结构及其应用,核素
专题:元素周期律与元素周期表专题
分析:(1)含有8个质子、10个中子、10个电子的离子,为氧离子;
(2)周期表中位于第8纵行的铁元素,在第四周期第ⅤⅢ族;
(3)周期表中最活泼的非金属元素为F.
(2)周期表中位于第8纵行的铁元素,在第四周期第ⅤⅢ族;
(3)周期表中最活泼的非金属元素为F.
解答:
解:(1)质子数为8,为O元素,该粒子的质量数为8+10=18,所以该粒子符号为
8X2-,故答案为:
8X2-;
(2)周期表中第8、9、10三个纵行为第Ⅷ族,铁元素,在第四周期第ⅤⅢ族,故答案为:ⅤⅢ;
(3)周期表中最活泼的非金属元素是F,位于第17纵行,第ⅦA族,故答案为:17;ⅦA.
18 |
18 |
(2)周期表中第8、9、10三个纵行为第Ⅷ族,铁元素,在第四周期第ⅤⅢ族,故答案为:ⅤⅢ;
(3)周期表中最活泼的非金属元素是F,位于第17纵行,第ⅦA族,故答案为:17;ⅦA.
点评:本题考查元素周期表的结构及应用,侧重于学生的分析能力和应用能力的考查,为高频考点,注意元素的位置及性质来解答,注重基础知识的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
可逆反应 H2 (g)+I2 (g)?2HI(g),温度一定,在1L的密闭容器中加入2molH2(g)和1molI2(g)开始反应,2min末测知容器中生成了1.2mol HI(g),下列说法正确的是( )
| A、H2(g)的消耗速率与I2(g)的生成速率始终相等 |
| B、反应过程中,H2(g)和I2(g)的转化率始终相等 |
| C、平衡前,正、逆反应速率的比值恒定 |
| D、反应开始至2min末,v(H2)=0.3mol?L-1?min-1 |
有机物A和B是正处于临床试验阶段的小分子抗癌药物,结构如图所示,关于有机物A和B的叙述,正确的是( )
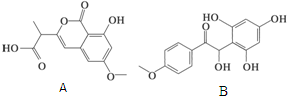

| A、二者都能与Br2发生反应,等物质的量A和B最多消耗的Br2的比例为2:3 |
| B、有机物A和B既可以与FeCl3溶液发生显色反应,又可以和NaHCO3溶液反应 |
| C、1 mol B最多能与6 mol氢气反应 |
| D、等物质的量A和B最多消耗的氢氧化钠质量比为1:1 |
下列各组物质之间不可能实现 X
Y
Z转化的是( )
| M |
| M |
| 选项 | X | Y | Z | M |
| A | C | CO | CO2 | O2 |
| B | Fe | FeCl2 | FeCl3 | Cl2 |
| C | AlCl3 | Al(OH)3 | NaAlO2 | NaOH |
| D | NH3 | NO | NO2 | O2 |
| A、A | B、B | C、C | D、D |
关于NaHCO3的性质,下列说法正确的是( )
| A、和酸反应放出等量的CO2所消耗的酸比Na2CO3多 |
| B、相同温度下溶解度比Na2CO3要大 |
| C、热稳定性比Na2CO3小 |
| D、NaHCO3只能和酸作用不能和碱作用 |
下列说法不正确的是 ( )
| A、用100mL的容量瓶准确量取100mL液体 |
| B、分液时,分液漏斗中下层液体从下口流出,上层液体从上口倒出 |
| C、用托盘天平称量NaCl固体时,NaCl放在称量纸上,称量NaOH固体时,NaOH放在小烧杯里 |