题目内容
 运用化学反应原理研究碳、氮的单质及其化合物的反应具有重要意义.
运用化学反应原理研究碳、氮的单质及其化合物的反应具有重要意义.(1)已知:N2(g)+O2(g)═2NO(g)△H1
N2(g)+3H2(g)?2NH3(g)△H2
2H2(g)+O2(g)═2H2O(g)△H3
则4NO(g)+4NH3(g)+O2(g)═4N2(g)+6H2O(g)△H=
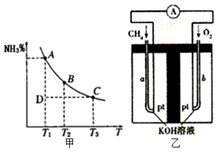
(2)在密闭容器中,一定条件下,进行如下反应:N2(g)+3H2(g)?2NH3(g)△H2,混合体系中NH3的百分含量和温度的关系如图甲所示(曲线上任何一点都表示平衡状态).根据图示回答下列问题:
①N2(g)+3H2(g)?2NH3(g)△H2
若在恒温、恒压条件下向上述平衡体系中通人氦气,平衡
②若温度为T1、T2,反应的平衡常数分别为K1,K2,则K1
(3)氨气溶于水得到氨水.已知常温下0.01mol?L-1的氨水中
| c(H+) |
| c(OH-) |
(4)碳氢化合物与氧气可形成新型燃料电池,如图乙所示以CH4为原料的燃料电池示意图.
①放电时,负极的电极反应式为
②假设装置中盛装100.0mL 3.0mol?L-1 KOH溶液,放电时参与反应的氧气在标准状况下体积为8960mL.放电完毕后,电解质溶液中各离子浓度的大小关系为
考点:用盖斯定律进行有关反应热的计算,常见化学电源的种类及其工作原理,化学平衡建立的过程,化学平衡的影响因素,弱电解质在水溶液中的电离平衡
专题:基本概念与基本理论
分析:(1)依据热化学方程式和盖斯定律计算出该反应的焓变;
(2)利用图示可知该反应随温度升高,产物(NH3)在体系中的百分含量降低,说明反应随温度升高向逆反应方向移动,确定反应的吸放热;在恒温、恒压下充入氦气,反应容器体积变大,压强减小,确定反应的移动方向;
(3)利用
=1×10-6,结合常温下Kw=c(H+)?c(OH-)=1×10-14可计算氨水溶液中c(H+),进而计算pH;NH3?H2O电离出阳离子的浓度等于溶液中OH-的浓度,根据Kb=
来计算;
(4)①负极是甲烷失电子发生氧化反应,根据电解质环境书写电极反应式;
②根据电池总反应式可知,当参与反应的氧气(标况下)8960mL时,有0.2molCH4参与反应,而电解质溶液中含有0.3molKOH,因此利用原子守恒知完全反应电解质溶液中的溶质为0.1molK2CO3、0.1molKHCO3,据此确定离子浓度的大小顺序.
(2)利用图示可知该反应随温度升高,产物(NH3)在体系中的百分含量降低,说明反应随温度升高向逆反应方向移动,确定反应的吸放热;在恒温、恒压下充入氦气,反应容器体积变大,压强减小,确定反应的移动方向;
(3)利用
| c(H+) |
| c(OH-) |
| c(NH4+)?c(OH-) |
| c(NH3?H2O) |
(4)①负极是甲烷失电子发生氧化反应,根据电解质环境书写电极反应式;
②根据电池总反应式可知,当参与反应的氧气(标况下)8960mL时,有0.2molCH4参与反应,而电解质溶液中含有0.3molKOH,因此利用原子守恒知完全反应电解质溶液中的溶质为0.1molK2CO3、0.1molKHCO3,据此确定离子浓度的大小顺序.
解答:
解:(1)已知:①N2(g)+O2(g)═2NO(g)△H1
②2(g)+3H2(g)?2NH3(g)△H2
③2H2(g)+O2(g)═2H2O(g)△H3
依据盖斯定律③×3-2×②-2×①得到,4NO(g)+4NH3(g)+O2(g)═4N2(g)+6H2O(g)△H=3△H3-2△H1-2△H2 kJ/mol,
故答案为:3△H3-2△H1-2△H2;
(2)①利用图示可知该反应随温度升高,产物(NH3)在体系中的百分含量降低,说明反应随温度升高向逆反应方向移动,故该反应的正反应为放热反应,即△H<0;在恒温、恒压下充入氦气,反应容器体积变大,反应向气体体积增大的逆反应方向移动,
故答案为:<、向左;
②因正反应为吸热反应,故升温反应逆向进行,反应进行程度减小,故K1>K2;由图示知,D点处的NH3百分含量比该温度下平衡时NH3的百分含量低,因此反应正向移动,即V(正)>v(逆),
故答案为:>;>;
(3)利用
=1×10-6,结合常温下Kw=c(H+)?c(OH-)=1×10-14可知该氨水溶液中c(H+)=1×10-10,故溶液pH=-lgc(H+)=10;结合NH3?H2O?NH4++OH-可知溶液中NH3?H2O电离出阳离子的浓度等于溶液中OH-的浓度,即c(NH4+)=1×10-4mol/L;利用混合液呈中性可推知溶液中c(NH4+)=c(Cl-)=
mol/L、c(NH3?H2O)=
mol/L,故Kb(NH3?H2O)=[c(NH4+)?c(0H-)]÷c(NH3?H2O)=[
×10-7]÷(
)=
.
故答案为:10;10-4 mol?L-1;K=
.
(4)①甲烷燃烧生成CO2与H2O,其中CO2又会进一步与电解质溶液KOH反应生成K2CO3与H2O,因此可写出负极(甲烷失电子发生氧化反应)反应式为:CH4-8e-+10OH-=CO32-+7H2O;
故答案为:CH4-8e-+10OH-=CO32-+7H2O;
②结合电池总反应式可知,当参与反应的氧气(标况下)8960mL时,有0.2molCH4参与反应,而电解质溶液中含有0.3molKOH,因此利用原子守恒知完全反应电解质溶液中的溶质为0.1molK2CO3、0.1molKHCO3,该溶液中CO32-水解程度大于HCO3-的电离,溶液呈碱性,故再结合溶质的物质的量可推知溶液中离子浓度大小关系为:c(K+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+),
故答案为:c(K+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+).
②2(g)+3H2(g)?2NH3(g)△H2
③2H2(g)+O2(g)═2H2O(g)△H3
依据盖斯定律③×3-2×②-2×①得到,4NO(g)+4NH3(g)+O2(g)═4N2(g)+6H2O(g)△H=3△H3-2△H1-2△H2 kJ/mol,
故答案为:3△H3-2△H1-2△H2;
(2)①利用图示可知该反应随温度升高,产物(NH3)在体系中的百分含量降低,说明反应随温度升高向逆反应方向移动,故该反应的正反应为放热反应,即△H<0;在恒温、恒压下充入氦气,反应容器体积变大,反应向气体体积增大的逆反应方向移动,
故答案为:<、向左;
②因正反应为吸热反应,故升温反应逆向进行,反应进行程度减小,故K1>K2;由图示知,D点处的NH3百分含量比该温度下平衡时NH3的百分含量低,因此反应正向移动,即V(正)>v(逆),
故答案为:>;>;
(3)利用
| c(H+) |
| c(OH-) |
| b |
| 2 |
| a-b |
| 2 |
| b |
| 2 |
| a-b |
| 2 |
| 10-7b |
| a-b |
故答案为:10;10-4 mol?L-1;K=
| 10-7b |
| a-b |
(4)①甲烷燃烧生成CO2与H2O,其中CO2又会进一步与电解质溶液KOH反应生成K2CO3与H2O,因此可写出负极(甲烷失电子发生氧化反应)反应式为:CH4-8e-+10OH-=CO32-+7H2O;
故答案为:CH4-8e-+10OH-=CO32-+7H2O;
②结合电池总反应式可知,当参与反应的氧气(标况下)8960mL时,有0.2molCH4参与反应,而电解质溶液中含有0.3molKOH,因此利用原子守恒知完全反应电解质溶液中的溶质为0.1molK2CO3、0.1molKHCO3,该溶液中CO32-水解程度大于HCO3-的电离,溶液呈碱性,故再结合溶质的物质的量可推知溶液中离子浓度大小关系为:c(K+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+),
故答案为:c(K+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+).
点评:本题综合考查学生热化学、电化学、溶液中离子浓度大小比较以及弱电解质的电离等方面的知识,注意知识的归纳和梳理是关键,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
向100mL18mol/L的H2SO4溶液中加入足量的铜片并加热,充分反应,再加入足量的锌片,充分反应后,被还原的H2SO4的物质的量( )
| A、小于0.9mol |
| B、等于0.9mol |
| C、在0.9mol与1.8mol之间 |
| D、等于1.8mol |
下列说法正确的是( )
| A、在AgNO3溶液中依次滴加同浓度的NaCl、Na2S溶液,可证明KSP(AgCl)>KSP(Ag2S) |
| B、△S>0的反应在一定条件下不一定可以自发进行 |
| C、以Al作阳极,Fe作阴极,可以实现铁上镀铝 |
| D、工业合成SO3不采用高压是因为增大压强对SO2的转化率影响不大 |
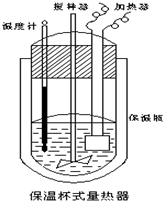 在如图所示的量热计中,将100mL 0.50mol?L-1CH3COOH溶液与100mL0.55mol?L-1NaOH 溶液混合,温度从25.0℃升高到27.7℃.已知量热计的热容常数(量热计各部件每升高1℃所需的热量)是150.5J?℃-1生成溶液的比热容为4.184J?g-1?℃-1,溶液的密度均近似为1g?mL-1.
在如图所示的量热计中,将100mL 0.50mol?L-1CH3COOH溶液与100mL0.55mol?L-1NaOH 溶液混合,温度从25.0℃升高到27.7℃.已知量热计的热容常数(量热计各部件每升高1℃所需的热量)是150.5J?℃-1生成溶液的比热容为4.184J?g-1?℃-1,溶液的密度均近似为1g?mL-1.