题目内容
7.X、Y、Z、W均为短周期主族元素且原子序数依次增大,其中X的气态氢化物的水溶液能够蚀刻玻璃,Y3+的硫酸盐水溶液显酸性,含Z2-的钠盐水溶液显碱性.下列说法正确的是( )| A. | 各元素在元素周期表中的族序数:W=X>Y>Z | |
| B. | 最高价氧化物对应的水化物的酸性:W>Z | |
| C. | 离子半径:X>Y>Z | |
| D. | YW3不能与NaOH溶液反应 |
分析 X、Y、Z、W均为短周期主族元素且原子序数依次增大,其中X的气态氢化物的水溶液能够蚀刻玻璃,则X为F元素;Y3+的硫酸盐水溶液显酸性,则Y为Al;含Z2-的钠盐水溶液显碱性,则Z为S元素,可推知W为Cl.
A.主族族序数等于最外层电子数;
B.元素非金属性越强,最高价氧化物对应水化物的酸性越强;
C.电子层结构相同的离子,核电荷数越大离子半径越小,离子电子层越多离子半径越大;
D.氯化铝与氢氧化钠反应生成氢氧化铝沉淀或偏铝酸钠.
解答 解:X、Y、Z、W均为短周期主族元素且原子序数依次增大,其中X的气态氢化物的水溶液能够蚀刻玻璃,则X为F元素;Y3+的硫酸盐水溶液显酸性,则Y为Al;含Z2-的钠盐水溶液显碱性,则Z为S元素,可推知W为Cl.
A.主族族序数等于最外层电子数,各元素在元素周期表中的族序数:Cl=F>S>Al,故A错误;
B.同周期自左而右元素非金属性增强,元素非金属性越强,最高价氧化物对应水化物的酸性越强,高氯酸的酸性比硫酸的强,故B正确;
C.电子层结构相同的离子,核电荷数越大离子半径越小,离子电子层越多离子半径越大,故离子半径S2->F->Al3,故C错误;
D.氯化铝与少量的氢氧化钠反应生成氢氧化铝沉淀与氯化钠,与过量的氢氧化钠反应生成偏铝酸钠与氯化钠,故D错误.
故选:B.
点评 本题考查结构性质位置关系应用,熟练掌握元素化合物知识,注意对元素周期律的理解,掌握微粒半径比较规律.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.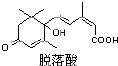 脱落酸是一种抑制生长的植物激素,因能促使叶子脱落而得名,其结构如图所示:则有关脱落酸的说法正确的是 ( )
脱落酸是一种抑制生长的植物激素,因能促使叶子脱落而得名,其结构如图所示:则有关脱落酸的说法正确的是 ( )
 脱落酸是一种抑制生长的植物激素,因能促使叶子脱落而得名,其结构如图所示:则有关脱落酸的说法正确的是 ( )
脱落酸是一种抑制生长的植物激素,因能促使叶子脱落而得名,其结构如图所示:则有关脱落酸的说法正确的是 ( )| A. | 脱落酸的化学式C15H18O4 | |
| B. | 脱落酸只能和醇类发生酯化反应 | |
| C. | 1 mol 脱落酸最多可以和2 mol 金属钠发生反应 | |
| D. | 1 mol 脱落酸最多可以和2 mol 氢气发生加成反应 |
2.A、B、C、D、E为周期表前20号主族元素,原子半径依次减小,其中A和E同族,A、B原子最外层电子数之比为1:4,A和C能形成一种既含离子键又含非极性共价键的化合物,A与C、B与E原子的电子层数都相差2.下列说法正确的是( )
| A. | D是非金属性最强的元素 | |
| B. | B的单质有多种同分异构体,其中一种是自然界中最坚硬的物质 | |
| C. | B的氢化物的稳定性大于D的氢化物 | |
| D. | A与C只能够形成两种化合物 |
4.高纯度的氢氧化镁广泛应用于医药、电力等领域.镁硅酸盐矿石可用于生产氢氧化镁,简要工艺流程如下:
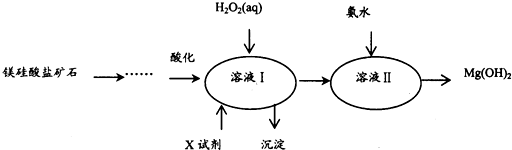
己知1:溶液I中除MgSO4外,还含有少量Fe3+、Al3+、Fe2+等离子
2:几种金属阳离子的氢氧化物沉淀时的pH如下表所示:
(1)Mg在周期表中的位置第三周期ⅡA族,Si的原子结构示意图为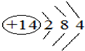 .
.
(2)向溶液I中加入X的作用是调节溶液pH.
(3)向溶液I中加入的两种试剂先后顺序是H2O2、MgO[Mg(OH)2或MgCO3](填化学式).
(4)加入H2O2溶液反应的离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O.
(5)如图是溶液Ⅱ中Mg2+转化率随温度t的变化示意图:
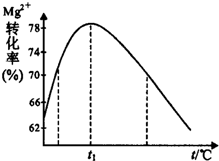
①向溶液Ⅱ中加入氨水反应的离子方程式是Mg2++2NH3•H2O=Mg(OH)2↓+2NH4+.
②t1前Mg2+转化率增大的原因是镁离子与氨水反应是吸热反应,升高温度,平衡右移,Mg2+转化率增大;t1后Mg2+转化率下降的原因是(用化学方程式表示)NH3•H2O$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O.

己知1:溶液I中除MgSO4外,还含有少量Fe3+、Al3+、Fe2+等离子
2:几种金属阳离子的氢氧化物沉淀时的pH如下表所示:
| Fe3+ | Al3+ | Fe2+ | Mg2+ | |
| 开始沉淀时 | 1.5 | 3.3 | 6.5 | 9.4 |
| 沉淀完全时 | 3.7 | 5.2 | 9.7 | 12.4 |
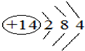 .
.(2)向溶液I中加入X的作用是调节溶液pH.
(3)向溶液I中加入的两种试剂先后顺序是H2O2、MgO[Mg(OH)2或MgCO3](填化学式).
(4)加入H2O2溶液反应的离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O.
(5)如图是溶液Ⅱ中Mg2+转化率随温度t的变化示意图:

①向溶液Ⅱ中加入氨水反应的离子方程式是Mg2++2NH3•H2O=Mg(OH)2↓+2NH4+.
②t1前Mg2+转化率增大的原因是镁离子与氨水反应是吸热反应,升高温度,平衡右移,Mg2+转化率增大;t1后Mg2+转化率下降的原因是(用化学方程式表示)NH3•H2O$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O.
1.下列实验能够获得成功的是( )
| A. | 检验溴乙烷中的溴:取溴乙烷加氢氧化钠溶液,加热,再加硝酸银溶液有浅黄色沉淀生成 | |
| B. | 检验葡萄糖:在硝酸银溶液中滴加稀氨水至沉淀恰好溶解再加少许葡萄糖溶液,水浴加热 | |
| C. | 检验乙醛:加入2% 硫酸铜溶液2 mL再加入2% NaOH溶液2 mL;加热至沸腾 | |
| D. | 实验室制乙烯:取浓硫酸和乙醇体积比1:3的溶液加热到170℃ |
2.在一定温度下的定容容器中,当下列物理量不再发生变化时,表明反应A(s)+2B(g)?C(g)+D(g) 已达到化学平衡状态的是( )
| A. | B的物质的量浓度 | B. | 混合气体的压强 | ||
| C. | 混合气体总物质的量 | D. | v(C)与v(D)的比值 |

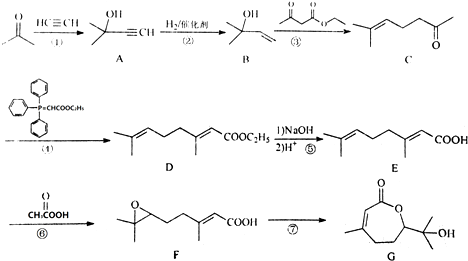
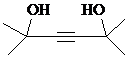 .
.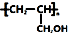 ,写出合成流程图(无机试剂任用).合成流程图示例如下:CH2=CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH.
,写出合成流程图(无机试剂任用).合成流程图示例如下:CH2=CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH.