题目内容
3.常温下,有关下列说法正确的是( )| A. | 与Al反应能放出H2的溶液中:Fe2+、K+、NO3-、SO42-能大量共存 | |
| B. | $\frac{{K}_{W}}{c({H}^{+})}$=1×10-13 mol•L-1的溶液中:NH4+、SO42-、NO3-能大量共存 | |
| C. | 苯酚钠溶液中通入少量CO2:CO2+H2O+2C6H5O-═2C6H5OH+CO32- | |
| D. | Fe3O4与稀HNO3反应:Fe3O4+8H+═Fe2++2Fe3++4H2O |
分析 A.与Al反应能放出H2的溶液,为非氧化性酸或强碱溶液;
B.$\frac{{K}_{W}}{c({H}^{+})}$=1×10-13 mol•L-1的溶液,显酸性;
C.反应生成苯酚和碳酸氢钠;
D.发生氧化还原反应生成硝酸铁、NO和水.
解答 解:A.与Al反应能放出H2的溶液,为非氧化性酸或强碱溶液,碱溶液中不能存在Fe2+,酸溶液中Fe2+(或Al)、H+、NO3-发生氧化还原反应不生成氢气,故A错误;
B.$\frac{{K}_{W}}{c({H}^{+})}$=1×10-13 mol•L-1的溶液,显酸性,该组离子之间不反应,可大量共存,故B正确;
C.反应生成苯酚和碳酸氢钠,离子反应为CO2+H2O+C6H5O-═C6H5OH+HCO3-,故C错误;
D.发生氧化还原反应生成硝酸铁、NO和水,离子反应为3Fe3O4+NO3-+28H+═9Fe3++NO↑+14H2O,故D错误;
故选B.
点评 本题考查离子共存及离子反应方程式的书写,为高频考点,把握离子之间的反应为解答的关键,侧重复分解反应、氧化还原反应的离子反应及共存考查,注重基础知识的夯实,题目难度不大.

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目
9.a、b、c、d为短周期元素,a的原子中只有1个电子,b2-和c+的电子层结构相同,d与b同族.下列叙述错误的是( )
| A. | a与其他三种元素形成的二元化合物中其化合价均为+1 | |
| B. | b与其他三种元素均可形成至少两种二元化合物 | |
| C. | c的原子半径是这些元素中最大的 | |
| D. | d与a形成的化合物的溶液呈弱酸性 |
6.已知异丙苯的结构简式如图,下列说法错误的是( )
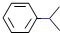

| A. | 异丙苯的分子式为C9H12 | |
| B. | 异丙苯的沸点比苯高 | |
| C. | 异丙苯中碳原子可能都处于同一平面 | |
| D. | 异丙苯和苯为同系物 |
12.下列叙述中正确的是( )
| A. | 共价化合物中一定没有离子键,离子化合物中一定没有共价键 | |
| B. | 金属原子与非金属原子间一定以共价键相结合 | |
| C. | 由不同种原子形成的纯净物一定是化合物 | |
| D. | 石墨转化成全刚石要吸收热量,石墨比金刚石稳定 |
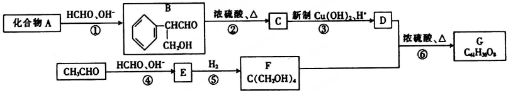
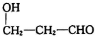
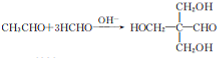 .
.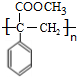 (填结构简式).
(填结构简式).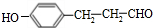 (填结构简式).
(填结构简式).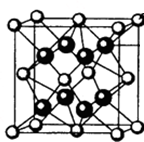 M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元素.M基态原子L层中p轨道电子数是s电子数的2倍,R是同周期元素中最活泼的金属元素,X和M形成的一种化合物是引起酸雨的主要大气污染物,Z的基态原子4s和3d轨道半充满.请回答下列问题:
M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元素.M基态原子L层中p轨道电子数是s电子数的2倍,R是同周期元素中最活泼的金属元素,X和M形成的一种化合物是引起酸雨的主要大气污染物,Z的基态原子4s和3d轨道半充满.请回答下列问题: