题目内容
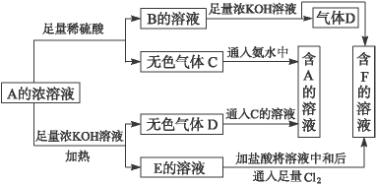
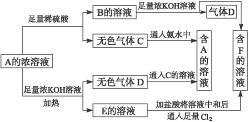
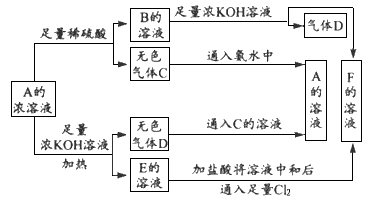
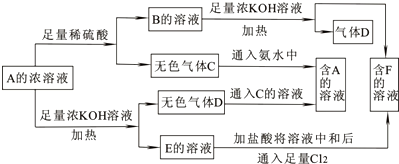
从物质A(某正盐)的水溶液出发有下图所示的一系列变化,其中气体D遇湿润红色石蕊试纸变蓝.完成下列离子反应方程式:
(1)B+KOH→D:______
(2)E→F:______.
解:气体D遇湿润红色石蕊试纸变蓝,则D为NH 3,B中含NH 4+,A与足量稀硫酸反应生成B和气体C,则A为弱酸的铵盐,B为NH4HSO 4,F为K2SO4,;A与足量的KOH反应生成E,E的溶液加足量盐酸中和后于氯气反应生成F,说明E为K2SO3,从而推出A为(NH4)2SO3、C为SO2.
(1)铵盐与碱反应生成氨气,反应的离子方程式为NH4++OH-=NH3↑+H2O,故答案为:NH4++OH-=NH3↑+H2O;
(2)在溶液中+4价的硫具有较强的还原性,可以被氯气氧化为+6价,反应的离子方程式为SO32-+Cl2+H2O=SO42-+2Cl-+2H+,
故答案为:SO32-+Cl2+H2O=SO42-+2Cl-+2H+
分析:气体D遇湿润红色石蕊试纸变蓝,则D为NH 3,B中含NH 4+,A与足量稀硫酸反应生成B和气体C,则A为弱酸的铵盐,B为NH4HSO 4,F为K2SO4,;A与足量的KOH反应生成E,E的溶液加足量盐酸中和后于氯气反应生成F,说明E为K2SO3,从而推出A为(NH4)2SO3、C为SO2.
点评:这种无机框图题,一定要找到突破口,再根据物质间的转换关系推断个物质.遇湿润红色石蕊试纸变蓝气体D是本题的突破口.
(1)铵盐与碱反应生成氨气,反应的离子方程式为NH4++OH-=NH3↑+H2O,故答案为:NH4++OH-=NH3↑+H2O;
(2)在溶液中+4价的硫具有较强的还原性,可以被氯气氧化为+6价,反应的离子方程式为SO32-+Cl2+H2O=SO42-+2Cl-+2H+,
故答案为:SO32-+Cl2+H2O=SO42-+2Cl-+2H+
分析:气体D遇湿润红色石蕊试纸变蓝,则D为NH 3,B中含NH 4+,A与足量稀硫酸反应生成B和气体C,则A为弱酸的铵盐,B为NH4HSO 4,F为K2SO4,;A与足量的KOH反应生成E,E的溶液加足量盐酸中和后于氯气反应生成F,说明E为K2SO3,从而推出A为(NH4)2SO3、C为SO2.
点评:这种无机框图题,一定要找到突破口,再根据物质间的转换关系推断个物质.遇湿润红色石蕊试纸变蓝气体D是本题的突破口.

练习册系列答案
相关题目