题目内容
对相同状况下的12C18O和14N2两种气体,下列说法正确的是
A.若质量相等,则质子数相等 B.若分子数相等,则体积相等
C.若原子数相等,则中子数相等 D.若体积相等,则密度相等
B
【解析】
试题分析:A、若两种气体质量相等,因为分子的相对分子质量不同,分子质量不同,分子的个数不同,又因为每个分子中含有相同的质子数是14,所以,两种气体的质子数不相等,A说法错误;B、因为相同状况下,体积相等的气体,含有相同的分子数,所以,若两种气体分子数相等,则体积相等,B正确;C.若两种气体的原子数相等,则两种气体的分子数也相同,由于一个12C18O分子和一个14N2分子中的中子数不同,所以,两种气体的中子数不相等,C错误;D、若两种气体体积相等,物质的量相等,但由于分子的质量不同,密度不相等,所以D说法错误,故选B。
考点:考查物质的量以及阿伏加德罗定律的有关应用与计算

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
下列有关实验操作、现象和解释或结论都正确的是
选项 | 实验操作 | 现象 | 解释或结论 |
A | 过量的Fe粉中加入稀HNO3,充分反应后,滴入KSCN溶液 | 溶液呈红色 | 稀HNO3将Fe氧化为Fe3+ |
B | AgI沉淀中滴入稀KCl溶液 | 有白色沉淀出现 | AgCl比AgI更难溶 |
C | Al箔插入稀HNO3中 | 无现象 | Al箔表面被HNO3氧化,形成致密的氧化膜 |
D | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |

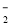 、CO
、CO