题目内容
 用如图所示的装置进行实验:
用如图所示的装置进行实验:(1)在实验开始前必须先做的实验操作是
(2)向试管a中加入10mL6mol/L的稀HNO3和1gCu片,立即用带有导管的橡皮塞塞紧试管口,请写出在试管a中有可能发生的反应的化学方程式
(3)实验过程中常常反应开始时速率缓慢,随后逐渐加快,这是由于
(4)欲较快地制得NO,可采取的措施是
A.加热 B.使用铜粉 C.稀释HNO3 D.改用浓HNO3.
考点:硝酸的化学性质,化学反应速率的影响因素
专题:
分析:(1)有气体参与的反应,必须检查装置的气密性;
(2)Cu和稀硝酸反应生成硝酸铜、NO和水,NO易被氧气氧化生成二氧化氮;
(3)温度越高,反应速率越快;反应物浓度越小,其反应速率越小;
(4)温度越高反应速率越快、接触面积越大反应速率越快.
(2)Cu和稀硝酸反应生成硝酸铜、NO和水,NO易被氧气氧化生成二氧化氮;
(3)温度越高,反应速率越快;反应物浓度越小,其反应速率越小;
(4)温度越高反应速率越快、接触面积越大反应速率越快.
解答:
解:(1)有气体参与的反应,必须检查装置的气密性,故答案为:检查装置的气密性;
(2)Cu和稀硝酸反应生成硝酸铜、NO和水,NO易被氧气氧化生成二氧化氮,所以涉及的反应方程式为3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O、2NO+O2=2NO2,
故答案为:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O、2NO+O2=2NO2;
(3)温度越高,反应速率越快;反应物浓度越小,其反应速率越小,该反应是放热反应,放出的热量使环境温度升高,所以反应速率加快,但随着反应的进行,硝酸的浓度降低,其反应速率减小,
故答案为:该反应放热,使温度升高,故反应速率加快;反应一段时间后HNO3浓度降低,故反应速率又逐渐减小;
(4)A.温度越高反应速率越快,所以升高温度增大反应速率,故A正确;
B.接触面积越大反应速率越快,所以使用铜粉增大反应速率,故B正确;
C.稀释硝酸,硝酸浓度减小,反应速率降低,故C错误;
D.使用浓硝酸,浓硝酸和铜反应生成二氧化氮而不是NO,故D错误;
故选AB.
(2)Cu和稀硝酸反应生成硝酸铜、NO和水,NO易被氧气氧化生成二氧化氮,所以涉及的反应方程式为3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O、2NO+O2=2NO2,
故答案为:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O、2NO+O2=2NO2;
(3)温度越高,反应速率越快;反应物浓度越小,其反应速率越小,该反应是放热反应,放出的热量使环境温度升高,所以反应速率加快,但随着反应的进行,硝酸的浓度降低,其反应速率减小,
故答案为:该反应放热,使温度升高,故反应速率加快;反应一段时间后HNO3浓度降低,故反应速率又逐渐减小;
(4)A.温度越高反应速率越快,所以升高温度增大反应速率,故A正确;
B.接触面积越大反应速率越快,所以使用铜粉增大反应速率,故B正确;
C.稀释硝酸,硝酸浓度减小,反应速率降低,故C错误;
D.使用浓硝酸,浓硝酸和铜反应生成二氧化氮而不是NO,故D错误;
故选AB.
点评:本题以铜和硝酸的反应为载体考查了影响反应速率的因素,明确温度、浓度、接触面积等对反应速率的影响,但决定物质反应速率的是物质本身的性质.

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案
相关题目
下列有机物的命名正确的是( )
A、 间二甲苯 间二甲苯 |
| B、2-甲基-2-丙烯 |
C、 2-甲基丁烷 2-甲基丁烷 |
| D、CH3-CHBr-CH2-CH33-溴丁烷Br |
下列关于元素周期表的说法正确的是( )
| A、能生成碱的金属元素都在ⅠA族 |
| B、稀有气体元素原子的最外层电子数均为8 |
| C、第二周期ⅣA族元素的原子核电荷数和种子数一定为6 |
| D、原子序数为14的元素位于元素周期表的第3周期ⅣA族 |
下列关于元素周期律和元素周期表的说法中正确的是( )
| A、目前发现的所有元素占据了周期表里全部位置,不可能再有新的元素被发现 |
| B、元素的性质随着原子序数的增加而呈周期性变化 |
| C、俄国化学家道尔顿为元素周期表的建立作出了巨大贡献 |
| D、最外层电子数为8的粒子是稀有气体元素的原子 |
下列化学用语书写正确的是( )
A、氯原子的结构示意图: | ||
B、H2O分子的比例模型: | ||
C、作为相对原子质量测定标准的碳核素:
| ||
D、用电子式表示氯化氢分子的形成过程: |
 与
与  ⑥CH3-CH2-OH和CH3-O-CH3
⑥CH3-CH2-OH和CH3-O-CH3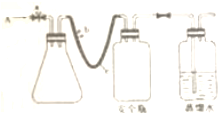 实验室用下列方法测定某水样中O2的含量
实验室用下列方法测定某水样中O2的含量