题目内容
下列说法符合事实的是( )
| A、电解硫酸铜溶液一段时间后,加入氯化钠固体不可能使溶液恢复到原来的浓度 |
| B、常温下由水电离产生的c(H+)=10-12mol/L的溶液中加入铝粉能够产生氢气 |
| C、已知Ksp(AgCl)=1.56×10-10.Ksp(Ag2CrO4)=9.0×10-12.在含Cl-、CrO42-浓度相同的溶液中滴加几滴稀AgNO3溶液时,则先生成AgCl沉淀 |
| D、在NaAlO2和Na2CO3的混合溶液中逐滴滴加盐酸直至过量,开始没有沉淀,随后产生沉淀,最后沉淀消失 |
考点:电解原理,水的电离,难溶电解质的溶解平衡及沉淀转化的本质,镁、铝的重要化合物
专题:基本概念与基本理论,元素及其化合物
分析:A、根据电解池的工作原理,要想让电解后的电解质复原,则遵循的原则是:出什么加什么;
B、常温下由水电离产生的c(H+)=10-12mol/L的溶液为酸或是碱溶液;
C、根据Ksp表达式计算得到的c(Ag+)越小,则越先生成沉淀;
D、恩局盐酸和混合物反映的先后顺序知识来回答判断.
B、常温下由水电离产生的c(H+)=10-12mol/L的溶液为酸或是碱溶液;
C、根据Ksp表达式计算得到的c(Ag+)越小,则越先生成沉淀;
D、恩局盐酸和混合物反映的先后顺序知识来回答判断.
解答:
解:A、电解硫酸铜溶液一段时间后,加入氧化铜或是碳酸铜或是氢氧化铜固体均可能使溶液恢复到原来的浓度,根据具体情况来确定,加入氯化钠固体不可能使溶液恢复到原来的浓度,故A正确;
B、常温下由水电离产生的c(H+)=10-12mol/L的溶液是酸或是碱溶液,如果是硝酸溶液时,向其中加入铝粉则不能够产生氢气,故B错误;
C、析出沉淀时,AgCl溶液中c(Ag+)=
,Ag2CrO4溶液中c(Ag+)=
,在含Cl-、CrO42-浓度相同的溶液中,则AgCl溶液中c(Ag+)小,则越先生成沉淀,所以种阴离子产生沉淀的先后顺序为Cl-、CrO42-,故C正确;
D、在NaAlO2和Na2CO3的混合溶液中逐滴滴加盐酸直至过量,先是发生反应AlO2-+H++H2O═Al(OH)3↓,AlO2-反应完毕,发生反应CO32-+H+═HCO3-,CO32-反应完毕,发生反应HCO3-+H+═CO2↑+H2O,最后发生反应Al(OH)3+3H+═Al3++3H2O,开始就会产生沉淀,故D错误.
故选AC.
B、常温下由水电离产生的c(H+)=10-12mol/L的溶液是酸或是碱溶液,如果是硝酸溶液时,向其中加入铝粉则不能够产生氢气,故B错误;
C、析出沉淀时,AgCl溶液中c(Ag+)=
| Ksp(AgCl) |
| c(Cl-) |
|
D、在NaAlO2和Na2CO3的混合溶液中逐滴滴加盐酸直至过量,先是发生反应AlO2-+H++H2O═Al(OH)3↓,AlO2-反应完毕,发生反应CO32-+H+═HCO3-,CO32-反应完毕,发生反应HCO3-+H+═CO2↑+H2O,最后发生反应Al(OH)3+3H+═Al3++3H2O,开始就会产生沉淀,故D错误.
故选AC.
点评:本题考查难溶电解质的溶解平衡、化学反应的先后顺序以及离子共存等方面的知识,注意知识的归纳和整理是关键,难度大.

练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目
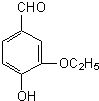 乙基香草醛是食品添加剂的增香原料,其结构简式如图所示,下列对该物质叙述正确的是( )
乙基香草醛是食品添加剂的增香原料,其结构简式如图所示,下列对该物质叙述正确的是( )| A、该物质可以进行消去反应 |
| B、该物质可以进行水解反应 |
| C、1mol该物质最多可与3 mol H2反应 |
| D、该物质可以和溴水发生取代反应 |
下列两种溶液:①pH=2的CH3COOH溶液;②pH=2的HCl溶液;相同条件下,有关上述溶液的比较中,正确的是( )
| A、溶液中的c(H+):①<② |
| B、分别中和等体积相同物质的量浓度的NaOH溶液,则消耗溶液的体积:①<② |
| C、等体积的①、②溶液分别与足量铝粉反应,生成H2的量:②>① |
| D、向等体积的两种溶液中分别加入100 mL水后,溶液的pH:①>② |
下列说法中,正确的是( )
| A、人们只能从有机物中取得有机化合物,不能利用无机物来合成有机物 |
| B、同分异构现象的广泛存在是有机物种类繁多的原因之一 |
| C、根据1H核磁共振谱就可以确定任何有机物分子的结构 |
| D、分子组成相差一个或若干个CH2原子团的化合物互称为同系物 |
下列表述中正确的是( )
| A、任何能使熵值增大的过程都能自发进行 |
| B、已知热化学方程式2SO2(g)+O2(g)?2SO3(g)△H=-Q kJ?mol-1(Q>0),则将2 mol SO2(g)和1 mol O2(g)置于一密闭容器中充分反应后放出Q kJ的热量 |
| C、化学平衡发生移动,平衡常数一定发生变化 |
| D、1 mol NaOH分别和1 mol CH3COOH、1 mol HNO3反应,后者比前者放出的热量多 |
下列各醇中,能发生消去反应生成 的是( )
的是( )
 的是( )
的是( )A、 |
| B、CH3-CH2-CH2-CH2OH |
C、 |
D、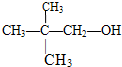 |
21世纪被认为是“海洋世纪”是人类大步走向海洋,开发利用海洋的世纪.下列有关海水资源的开发利用说法正确的是( )
| A、在研究和开发海洋资源时,不能以牺牲环境为代价 |
| B、海水中含有溴元素,可以直接萃取得到溴单质 |
| C、海水中的铀含量极低,从海水中提铀是十分不经济的行为 |
| D、在研究和开发海洋资源时,必要时可以以牺牲环境为代价 |
在标准状况下,如果1.6L氧气含n个氧分子,则阿伏加德罗常数的数值为( )
| A、28n | B、14n |
| C、n/28 | D、n/14 |