题目内容
(6分)一定量的氢气在氯气中燃烧,所得混合物用100mL 6.00mol/L的NaOH溶液(密度为1. 2g/mL)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.1000mol。
(1)原NaOH溶液的质量分数为
(2)所得溶液中Cl-的物质的量为 mol
(3)所用氯气和参加反应的氢气的物质的量之比n(Cl2) :n(H2)= 。
(1)20. 0% (2)0. 5 (3)3︰2
【解析】
试题分析:(1)利用物质的量浓度与溶液的质量分数的换算关系式 可得原NaOH溶液的质量分数为(6×40)÷(1000×1.2)=20. 0%;由于反应后产物只有NaCl、NaClO的形式。根据元素守恒可得n(NaCl)+ n(NaClO)=n(NaOH),所以n(NaCl) =n(NaOH)-n(NaClO)=0.1L×6mol/L-0.1000mol=0.5mol;发生反应Cl2+2NaOH=NaCl+NaClO+H2O的氯气的物质的量是n(Cl2)= n(NaClO)=0.1mol,则发生反应Cl2+H2
可得原NaOH溶液的质量分数为(6×40)÷(1000×1.2)=20. 0%;由于反应后产物只有NaCl、NaClO的形式。根据元素守恒可得n(NaCl)+ n(NaClO)=n(NaOH),所以n(NaCl) =n(NaOH)-n(NaClO)=0.1L×6mol/L-0.1000mol=0.5mol;发生反应Cl2+2NaOH=NaCl+NaClO+H2O的氯气的物质的量是n(Cl2)= n(NaClO)=0.1mol,则发生反应Cl2+H2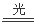 2HCl;HCl+NaOH=NaCl+H2O的氯气的物质的量是n(Cl2)=[(0.1L×6.00mol/L)-2n(NaClO)]÷2=0.2mol,所以反应的氢气的物质的量也是0.2mol,故所用氯气和参加反应的氢气的物质的量之比n(Cl2) :n(H2)=(0.1mol+0.2mol):0.2mol=3:2。
2HCl;HCl+NaOH=NaCl+H2O的氯气的物质的量是n(Cl2)=[(0.1L×6.00mol/L)-2n(NaClO)]÷2=0.2mol,所以反应的氢气的物质的量也是0.2mol,故所用氯气和参加反应的氢气的物质的量之比n(Cl2) :n(H2)=(0.1mol+0.2mol):0.2mol=3:2。
考点:考查溶液的物质的量浓度与质量分数的换算、氯气与氢气混合反应后的产物与NaOH反应的知识。

练习册系列答案
相关题目