题目内容
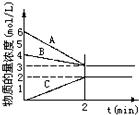 已知某一化学反应情况如图,请回答
已知某一化学反应情况如图,请回答(1)2分钟内A的平均速率是
(2)该反应方程式为
考点:化学平衡建立的过程
专题:图示题
分析:(1)根据v=
计算反应速率;
(2)根据在反应中,反应物的浓度减小,生成物的浓度增加,变化的浓度之比等于反应中计量数之比,写出化学方程式;
| △c |
| t |
(2)根据在反应中,反应物的浓度减小,生成物的浓度增加,变化的浓度之比等于反应中计量数之比,写出化学方程式;
解答:
解:(1)根据图可知,2分钟内A减小了6mol/L-3mol/L=3mol,所以A平均反应速率为
=1.5 mol/(L?min),故答案为:1.5 mol/(L?min);
(2)根据图可知,A浓度减小了(6-3)mol/L=3mol/L,B浓度减小了(4-3)mol/L=1mol/L,所以A、B为反应物,C的浓度增加了2mol/L,所以C为生成物,A、B、C的变化量之比为3:1:2,反应中各物质计量数之比等于物质的浓度的变化量之比,所以化学方程式为3A+B?2C,故答案为:3A+B?2C;
| 3mol/L |
| 2min |
(2)根据图可知,A浓度减小了(6-3)mol/L=3mol/L,B浓度减小了(4-3)mol/L=1mol/L,所以A、B为反应物,C的浓度增加了2mol/L,所以C为生成物,A、B、C的变化量之比为3:1:2,反应中各物质计量数之比等于物质的浓度的变化量之比,所以化学方程式为3A+B?2C,故答案为:3A+B?2C;
点评:本题主要考查了根据图写化学方程式,化学反速率的计算,难度较小,都是一些基础内容.

练习册系列答案
相关题目
通常情况下,将10g下列固体与90mL水充分混合,所得溶液的物质的量浓度最低的是( )
| A、CuSO4?5H2O |
| B、Na2O |
| C、CaO |
| D、KNO3 |
设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A、常温常压下,46 g NO2与N2O4的混合气体中含有的分子总数为NA |
| B、0.1 mol乙烯和乙醇的混合物完全燃烧所消耗O2的分子数为0.3 NA |
| C、25℃时,pH=13的Ba(OH)2溶液中含有OH-的数目为0.1 NA |
| D、一定量的钠与8 g氧气作用,若两者均无剩余,转移的电子数为NA |