题目内容
20.SO2在400~600℃下的催化氧化:2SO2+O2?2SO3,这是一个正反应放热的可逆反应.如果反应在密闭容器中进行,下述有关说法中正确的是( )| A. | 使用催化剂是为了加快反应速率,提高生产效率 | |
| B. | 通过调控反应条件,SO2可以100%地转化为SO3 | |
| C. | SO2的浓度与SO3的浓度相等时,反应达到平衡 | |
| D. | 因为反应放热,所以升高温度会使反应速率减慢 |
分析 该反应是前后气体体积减小的放热反应,根据外界条件对化学平衡的影响因素分析;
A、催化剂加快反应速率,提高生产效率,不改变化学平衡;
B、反应是可逆反应分析判断;
C、依据平衡标志分析判断;
D、升温增大反应速率.
解答 解:该反应是前后气体体积减小的放热反应.
A、使用催化剂加快了反应速率,缩短反应时间,提高生产效率,故A正确;
B、该反应是可逆反应,所以该反应存在反应限度,反应物不可能100%的转化,故B错误;
C、达到平衡时,SO2的浓度与SO3的浓度可能相等,也可能不相等,要依据反应物的初始浓度及转化率,故C错误;
D、温度对化学反应速率影响是温度升高,任何反应速率增大,只是平衡逆向进行,故D错误;
故选A.
点评 本题考查了影响化学平衡移动的因素,难度不大,注意影响化学反应速率和化学平衡的影响因素分析判断.

练习册系列答案
相关题目
11.下列化合物在一定条件下,既能发生消去反应,又能发生水解反应的是( )
| A. | CH3Cl | B. | 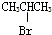 | C. | (CH3)3C-CH2Cl | D. | 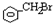 |
8.下列说法正确的是( )
| A. | 石油是混合物,其分馏产品汽油为纯净物 | |
| B. |  的核磁共振氢谱中有4种峰 的核磁共振氢谱中有4种峰 | |
| C. | 苯甲酸的重结晶实验中,粗苯甲酸溶解后还要加点水的目的是减少过滤时苯甲酸的损失 | |
| D. | 苯中滴加浓溴水,充分震荡后溴水层褪色,是因为苯与溴水中的溴发生了加成反应 |
5.下表中对应关系正确的是( )
| A | CH3CH3+Cl2$\stackrel{光}{→}$CH3CH2Cl+HCl CH2═CH2+HCl-→CH3CH2Cl | 均为取代反应 |
| B | 甲烷的燃烧 乙烯使酸性高锰酸钾溶液褪色 | 有机物均发生了 氧化反应 |
| C | Cl2+2Br-═2Cl-+Br2 Zn+Cu2+═Zn2++Cu | 均为单质被还原的 置换反应 |
| D | 2Na2O2+2H2O═4NaOH+O2↑ Cl2+H2O?HCl+HClO | 均为水作还原剂的 氧化还原反应 |
| A. | A | B. | B | C. | C | D. | D |
12.化学工业在经济发展中的作用举足轻重,下列有关工业生产的叙述中,正确的是( )
| A. | 硫酸生产中常采用催化剂提高SO2的转化率 | |
| B. | 合成氨中采用及时分离氨气提高反应速率 | |
| C. | 电镀铜时,溶液中c(Cu2+)基本保持不变 | |
| D. | 用电解熔融氧化镁的方法制取镁 |
9.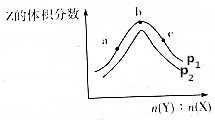 一定温度下,某密闭容器中存在反应:X(g)+2Y(g)?2Z(g),测得平衡体系中Z的体积分数与体系的压强(p)、投料比[b(Y):n(X)]关系如图所示,下列分析一定正确的是( )
一定温度下,某密闭容器中存在反应:X(g)+2Y(g)?2Z(g),测得平衡体系中Z的体积分数与体系的压强(p)、投料比[b(Y):n(X)]关系如图所示,下列分析一定正确的是( )
 一定温度下,某密闭容器中存在反应:X(g)+2Y(g)?2Z(g),测得平衡体系中Z的体积分数与体系的压强(p)、投料比[b(Y):n(X)]关系如图所示,下列分析一定正确的是( )
一定温度下,某密闭容器中存在反应:X(g)+2Y(g)?2Z(g),测得平衡体系中Z的体积分数与体系的压强(p)、投料比[b(Y):n(X)]关系如图所示,下列分析一定正确的是( )| A. | p2>p1 | B. | Y的转化率:a<c<b | ||
| C. | b点时n(Y):n(X)=2 | D. | 该反应是一个放热反应 |
 表示的分子式C7H12;名称是3-甲基-2,4-己二烯.
表示的分子式C7H12;名称是3-甲基-2,4-己二烯.