题目内容
14.关于下列四个图象的说法中正确的是( )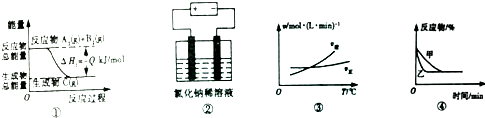
| A. | 图①表示可逆反应A2(g)+B2(g)?C(g)的△H1大于0 | |
| B. | 图②是电解氯化钠稀溶液的电解池,其中阴、阳极产生气体的体积之比一定为1:1 | |
| C. | 图③表示可逆反应A2(g)+3B2(g)?2AB3(g)的△H小于0 | |
| D. | 图④表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)的影响,乙曲线对应的压强大 |
分析 A.图①反应物总能量大于生成物总能量,反应放热;
B.图②电解氯化钠稀溶液,阳极开始生成Cl2,之后生成O2;
C.图③随着温度的升高,逆反应速率大于正反应速率,平衡向逆方向进行;
D.图④表示催化剂对可逆反应的影响.
解答 解:A.图①反应物总能量大于生成物总能量,反应放热,则△H小于0,故A错误;
B.图②电解氯化钠稀溶液,阳极开始生成Cl2,之后生成O2,如电解时间较长,则阴、阳极产生气体体积之比大于1:1,故B错误;
C.图③随着温度的升高,逆反应速率大于正反应速率,平衡向逆方向进行,说明反应放热,则△H小于0,故C正确;
D.图④中甲乙两途径平衡状态相同,则应是催化剂对可逆反应的影响,故D错误.
故选C.
点评 本题考查较为综合,题目难度中等,易错点为B,注意点解氯化钠稀溶液的特点,正确判断两极反应是解答该题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.美国“海狼”潜艇上的核反应堆内使用了液体铝钠合金(单质钠和单质铝熔合而成)作载热介质,有关说法不正确的是( )
| A. | 铝钠合金的熔点比铝低 | |
| B. | 铝钠合金若投入一定的水中可得无色溶液,则n(Al)≤n(Na) | |
| C. | 铝钠合金投入到足量氯化铜溶液中,肯定有氢氧化铜沉淀也可能有铜析出 | |
| D. | m g不同组成的铝钠合金投入足量盐酸中,放出的H 2 越多,则铝的质量分数越小 |
2.下列性质的比较中,不正确的是( )
| A. | 稳定性:Na2CO3>NaHCO3 | B. | 熔点:生铁>纯铁 | ||
| C. | 酸性:H2CO3>HClO | D. | 氧化性:Fe3+>Cu2+ |
9.某无色溶液与Al反应能放出H2,下列离子在该溶液中一定能大量共存的是( )
| A. | NH4+、Fe2+、Cl-、SO42- | B. | Na+、K+、Cl-、SO42- | ||
| C. | Mg2+、AlO2-、Cl-、SO42- | D. | K+、Ca2+、HCO3-、Cl- |
19.氯化硼的熔点为-107℃、沸点为12.5℃,在氯化硼分子中,氯-硼-氯键角为120°,它可以水解,水解产物之一是氯化氢,下列对氯化硼的叙述中正确的是( )
| A. | 氯化硼是原子晶体 | |
| B. | 熔化时,氯化硼能导电 | |
| C. | 硼原子以sp3杂化 | |
| D. | 水解方程式:BCl3+3H2O═H3BO3+3HCl |
6.绿矾(FeSO4•7H2O)广泛用于工农业生产.下面是以市售铁屑(含少量锡、氧化铁等杂质)为原料生成纯净绿矾的一种方法:
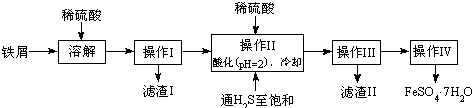
查询资料,得有关物质的数据如下表:
(1)操作II中,通入硫化氢至饱和的目的是除去Sn2+并防止Fe2+被氧化;在溶液中用硫酸酸化至pH=2的目的是防止Fe2+沉淀;
(2)操作IV得到的绿矾晶体用少量冰水洗涤,其洗涤的目的是洗去晶体表面的硫酸等杂质;用冰水的原因是降低晶体的溶解度,减少溶解导致FeSO4•7H2O的损耗;
(3)次氯酸盐在碱性条件下氧化硫酸亚铁可得高冷净水剂K2FeO4,离子方程式为2ClO-+Fe2++4OH-=FeO42-+2Cl-+2H2O;
(4)25℃时,将FeSO4•7H2O样品溶于水配成FeSO4溶液,该溶液中的Fe2+在空气中易被氧化成Fe3+,若向完全被氧化后的溶液中滴加NaOH溶液,当滴至溶液的pH=4时,溶液中的c(Fe3+)=4.0×10-8mol/L.[已知该温度下,Fe(OH)3的Ksp=4.0×10-38]
(5)将8.34gFeSO4•7H2O样品隔绝空气加热脱水,其重曲线(样品质量随温度变化的曲线)如图所示: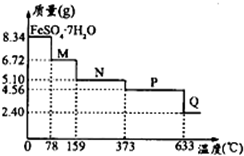
①在100℃时M的化学式为FeSO4•4H2O;
②FeSO4•7H2O晶体中有3种不同结合力的水分子.

查询资料,得有关物质的数据如下表:
| 25℃时 | pH值 |
| 饱和H2S溶液 | 3.9 |
| SnS沉淀完全 | 1.6 |
| FeS开始沉淀 | 3.0 |
| FeS沉淀完全 | 5.5 |
(2)操作IV得到的绿矾晶体用少量冰水洗涤,其洗涤的目的是洗去晶体表面的硫酸等杂质;用冰水的原因是降低晶体的溶解度,减少溶解导致FeSO4•7H2O的损耗;
(3)次氯酸盐在碱性条件下氧化硫酸亚铁可得高冷净水剂K2FeO4,离子方程式为2ClO-+Fe2++4OH-=FeO42-+2Cl-+2H2O;
(4)25℃时,将FeSO4•7H2O样品溶于水配成FeSO4溶液,该溶液中的Fe2+在空气中易被氧化成Fe3+,若向完全被氧化后的溶液中滴加NaOH溶液,当滴至溶液的pH=4时,溶液中的c(Fe3+)=4.0×10-8mol/L.[已知该温度下,Fe(OH)3的Ksp=4.0×10-38]
(5)将8.34gFeSO4•7H2O样品隔绝空气加热脱水,其重曲线(样品质量随温度变化的曲线)如图所示:

①在100℃时M的化学式为FeSO4•4H2O;
②FeSO4•7H2O晶体中有3种不同结合力的水分子.
3.把500mL含BaCl2和KCl的混合溶液分成两等份,向其中一份中加入含a mol硫酸钠的溶液,恰好使钡离子完全沉淀;向另一份中加入含b mol硝酸银的溶液,恰好使氯离子完全沉淀.则该混合溶液中钾离子浓度为( )
| A. | 0.25(b-2a)mol/L | B. | 4(2a-b)mol/L | C. | 2(b-2a)mol/L | D. | 4(b-2a)mol/L |