题目内容
下列说法正确的是( )
| A、酸、碱和盐类都属于电解质,其他化合物都是非电解质 |
| B、强电解质与弱电解质的本质区别,是其水溶液导电性的减弱 |
| C、电解质与非电解质的本质区别,是在水溶液或熔化状态下能否电离 |
| D、常见的强酸、强碱和大部分盐都是强电解质,其他化合 物都是非电解质 |
考点:电解质与非电解质,强电解质和弱电解质的概念
专题:电离平衡与溶液的pH专题
分析:水溶液中或熔融状态下能够导电的化合物称为电解质;在上述两种情况下都不能导电的化合物称为非电解质,蔗糖、乙醇等都是非电解质.大多数的有机物都是非电解质;在溶液中能够完全电离的电解质为强电解质,不能完全电离的为弱电解质,据此进行解答.
解答:
解:A.电解质为在溶液中或熔融状态下能够导电的化合物,除了酸、碱和盐还有其他化合物,故A错误;
B.强电解质与弱电解质的本质区别是能否完全电离,与其水溶液导电性的强弱无必然联系,故B错误;
C.电解质与非电解质的本质区别,是在水溶液或熔化状态下能否电离,故C正确;
D.在溶液中能够完全电离的电解质为强电解质,包括强酸、强碱和大部分盐、其他化合物,故D错误;故选C.
B.强电解质与弱电解质的本质区别是能否完全电离,与其水溶液导电性的强弱无必然联系,故B错误;
C.电解质与非电解质的本质区别,是在水溶液或熔化状态下能否电离,故C正确;
D.在溶液中能够完全电离的电解质为强电解质,包括强酸、强碱和大部分盐、其他化合物,故D错误;故选C.
点评:本题考查了电解质与非电解质、强电解质与弱电解质的判断,题目难度不大,注意掌握电解质与非电解质、强电解质与弱电解质的概念及判断方法,明确电解质和非电解质都一定为化合物,单质和混合物既不是电解质,也不是非电解质.

练习册系列答案
相关题目
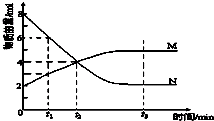 一定温度下在2L的密闭容器内进行反应,M、N的物质的量随反应时间变化的曲线如图,下列表述正确的是( )
一定温度下在2L的密闭容器内进行反应,M、N的物质的量随反应时间变化的曲线如图,下列表述正确的是( )| A、反应的化学方程式:2M?N |
| B、t2时,正、逆反应速率相等,达到平衡 |
| C、平衡时,N的转化率为75% |
| D、若t1=2min,用N的浓度表示的化学反应速率为0.5 mol?(L?s)-1 |
下列有关化学能与热能的说法错误的是( )
| A、燃烧反应都属于放热反应 |
| B、化学反应必然伴随着能量的变化 |
| C、吸热反应是指需要加热才能进行的反应 |
| D、化学键的断裂和形成是化学反应中能量变化的主要原因 |
下列说法不正确的是( )
| A、二氧化硅是制造光导纤维的材料,单质硅是良好的半导体材料 |
| B、SiO2和CO2都是酸性氧化物,但SiO2不能和水反应生成硅酸 |
| C、保存NaOH溶液时不能用玻璃塞 |
| D、二氧化硅性质稳定,不与任何酸反应 |
在标准状况下,13g某气体的分子数与14gCO的分子数相等,此气体的相对分子质量是( )
| A、34 | B、52 | C、36 | D、26 |
下列说法正确的是( )
A、已知0.1mol?L-1的醋酸溶液中存在电离平衡:CH3COOH?CH3COO-+H+,加少量烧碱溶液可使溶液中
| ||
| B、25℃时,向水中加入少量固体CH3COONa,水的电离平衡:H2O?H++OH-逆向移动,c(H+)降低 | ||
| C、取c(H+)=0.01mol?L-1的盐酸和醋酸各100mL,分别稀释2倍后,再分别加入0.03 g锌粉,在相同条件下充分反应,醋酸与锌反应的速率大 | ||
| D、向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液中:c(Na+)<c(NO3-) |
一些不法商人在面粉生产中添加过氧化钙(CaO2)等添加剂对食品进行增白.下列关于过氧化钙(CaO2)的叙述正确的是( )
| A、CaO2中阴、阳离子的个数比为1:1 |
| B、CaO2对面粉增白原理与SO2漂白原理相似 |
| C、CaO2和水反应时,每产生1molO2转移电子4mol |
| D、CaO2放入NaHCO3溶液中,会放出二氧化碳,并产生白色浑浊 |
下列说法正确的是( )
| A、HF、HCl、HBr、HI的热稳定性依次减弱,沸点却依次升高 |
| B、熔融状态下能导电的化合物一定含离子键 |
| C、H2O2分子中所有的原子均为8电子稳定结构 |
| D、NaHSO4晶体中阴、阳离子的个数是1:2且熔化时破坏的是离子键和共价键 |
下列属于强电解质的是( )
①NaOH;②NH3?H2O;③CaCO3;④CH3COOH;⑤NaHCO3;⑥Al(OH)3;⑦NH4Cl;⑧CO2;⑨CH3CH2OH(乙醇);⑩Cu.
①NaOH;②NH3?H2O;③CaCO3;④CH3COOH;⑤NaHCO3;⑥Al(OH)3;⑦NH4Cl;⑧CO2;⑨CH3CH2OH(乙醇);⑩Cu.
| A、①③⑥⑦ | B、②④⑥⑦ |
| C、①③⑤⑦ | D、除⑧⑨⑩外 |