题目内容
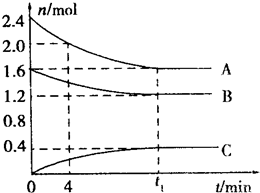 T℃时,在一容积为2L的容器中,A气体和B气体反应生成C气体,反应过程中A、B、C浓度变化如图所示:
T℃时,在一容积为2L的容器中,A气体和B气体反应生成C气体,反应过程中A、B、C浓度变化如图所示:①写出该反应的化学方程式:
②已知K(300℃)>K(500℃),该反应的正反应方向是
③若增大压强,则A的转化率会
考点:物质的量或浓度随时间的变化曲线
专题:化学平衡专题
分析:①根据物质的量的变化比例写出化学方程式;
②根据化学平衡常数表达式判断;
③反应前气体体积大于反应后气体体积,以此判断.
②根据化学平衡常数表达式判断;
③反应前气体体积大于反应后气体体积,以此判断.
解答:
解:①A物质的量减小了2.4mol-1.6mol=0.8mol,为反应物,B物质的量减小了1.6mol-1.2mol=0.4mol,为反应物,C物质的量增大了0.4mol,为生成物,计量数之比为:2:1:1,且存在化学平衡状态,化学方程式为:2A+B?C,故答案为:2A+B?C;
②化学平衡常数为生成物浓度系数次幂的乘积与反应物浓度系数次幂乘积的比值,由于K(300℃)>K(500℃),即温度升高化学平衡向逆反应方向移动,正反应方向放热,故答案为:放热;
③反应前气体体积大于反应后气体体积,增大压强化学平衡向正反应方向移动,A的转化率增大,故答案为:增大.
②化学平衡常数为生成物浓度系数次幂的乘积与反应物浓度系数次幂乘积的比值,由于K(300℃)>K(500℃),即温度升高化学平衡向逆反应方向移动,正反应方向放热,故答案为:放热;
③反应前气体体积大于反应后气体体积,增大压强化学平衡向正反应方向移动,A的转化率增大,故答案为:增大.
点评:本题考查化学平衡图象、化学方程式书写、影响平衡的因素等,难度不大.

练习册系列答案
相关题目
下列关于有机物的说法中正确的( )
A、新药帕拉米韦对禽流感H7N9有显著疗效,它的结构简式为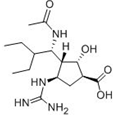 化学式是C15H26N4O4 化学式是C15H26N4O4 |
| B、2013年11月20日山东现‘夺命快递’----化学品泄漏致1死7中毒.该化学品为氟乙酸甲酯它是无色透明液体,溶于乙醇、乙醚,不溶于水.它属于酯类,也属于卤代烃 |
C、绿原酸的结构简式为: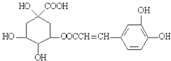 ,它在一定条件下能发生氧化、加成、酯化、水解、消去、加聚、缩聚反应 ,它在一定条件下能发生氧化、加成、酯化、水解、消去、加聚、缩聚反应 |
D、苯的同系物 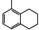 ,其所有碳原子不可能在同一平面上 ,其所有碳原子不可能在同一平面上 |
下列叙述不正确的是( )
| A、可用溴水鉴别直馏汽油与裂化汽油 |
| B、铜丝灼烧法可定性确定有机物中是否存在卤素 |
| C、德国化学家维勒提出了有机化学的概念 |
| D、CH3CH=CHCH(CH3)CH=CHCH3中不存在对映异构体,但存在顺反异构 |
 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表: 如图所示的两个实验装置中,均为500mL氯化铜溶液,试回答下列问题:
如图所示的两个实验装置中,均为500mL氯化铜溶液,试回答下列问题: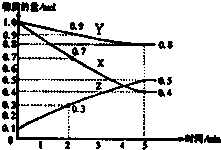 化学反应速率与生产、生活密切相关.
化学反应速率与生产、生活密切相关. 则乙醇发生酯化反应时,断裂的键是
则乙醇发生酯化反应时,断裂的键是 ②CH2=CH2③CH≡CH ④
②CH2=CH2③CH≡CH ④ -CH2OH⑤
-CH2OH⑤ -CH3⑥CH3COO-
-CH3⑥CH3COO- ⑦CH3CH2CH2CH2Br中属于芳香烃的是
⑦CH3CH2CH2CH2Br中属于芳香烃的是