题目内容
4.下列叙述中正确的是( )| A. | 摩尔是把物质的质量和微观粒子数联系起来的一个基本物理量 | |
| B. | 1摩尔H2SO4的质量为98g/mol | |
| C. | 国际上规定,0.012 kg 碳原子所含有的碳原子数目为 1 mol | |
| D. | 1摩尔氢气分子可以表示为1mol H2 |
分析 A.摩尔是物质的量的单位;
B.质量单位是g,n=$\frac{m}{M}$计算质量;
C.碳原子指含有6个质子6个中子的原子,本选项未明确;
D.物质的量需要指明微粒种类,分子可以用化学式表示;
解答 解:A.物质的量是把物质的质量和微观粒子数联系起来的一个基本物理量,摩尔是物质的量的单位,故A错误;
B.1摩尔H2SO4的质量为98g,故B错误;
C.是以12C所含有的碳原子数为标准,即0.012kg12C所含有的碳原子数目为1mol,故C错误;
D.物质的量表示的是微观粒子的物理量,需要指明所表示的微粒种类,1摩尔氢气分子可以表示为1molH2,故D正确;
故选D.
点评 本题考查物质的量的单位,摩尔是单位不是物理量,质量与摩尔质量的单位易混淆,微粒的指定要有明确性,这些都是化学用语使用不规范,题目较简单.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
14.某一元弱酸HA的相对分子质量为M.在t℃时,将ag HA完全溶解于水中,得V mL饱和溶液,测得该溶液的密度为ρ g/cm3,其中溶液pH=b.下列叙述中,错误的是( )
| A. | t℃时,HA的Ka=10-2b/1000a/MV | |
| B. | 物质的量浓度:c(HA)=1000a/MV mol•L-1 | |
| C. | t℃时,HA的溶解度:S=100a/ρV g | |
| D. | HA的质量分数:ω(HA)=(a/ρV)×100% |
15.一定条件下反应N2+3H2?2NH3达平衡,当单独改变下述条件后有关叙述一定错误的是( )
| A. | 加催化剂,v(正)和v(逆)都发生变化,且变化的倍数相等 | |
| B. | 加压,v(正)和v(逆)都增大,且v(正)增加倍数大于v(逆)增加倍数 | |
| C. | 降温,v(正)和v(逆)都减少,且v(正)减少倍数大于v(逆)减少倍数 | |
| D. | 增加c(N2),v(正)和v(逆)都增大,且v(正)增加倍数大于v(逆)增加倍数 |
12.下列离子方程式表达正确的是( )
| A. | NaHSO4溶液中滴加入Ba(OH)2溶液至中性H++Ba2++OH-+SO42-═BaSO4↓+H2O | |
| B. | 酸性KMnO4溶液与双氧水反应:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O | |
| C. | 钢铁腐蚀时可能发生的正极反应为:4OH-+4e-═2H2O+O2↑ | |
| D. | 将氯气溶于水制备次氯酸:Cl2+H2O?2H++Cl-+ClO- |
19.将Cu片放入0.1mol/LFeCl3溶液中,反应一定时间后取出Cu片,所得溶液Q中的c(Fe3+):c(Fe2+)=2:3,下列有关说法中正确的是( )
| A. | 反应中转移电子为0.04 mol | B. | Q中n(Cu2+):n(Fe2+)=1:2 | ||
| C. | 溶液Q比原溶液增重了 1.28 g | D. | 3c(Fe3+)+2c(Fe2+)+2c(Cu2+)=0.1 mol/L |
9.常温下,下列溶液中微粒的物质的量浓度关系正确的是( )
| A. | 将等体积、等物质的量浓度的CH3COONH4与CH3COONa溶液混合:c(CH3COO-)>c(Na+)>c(NH4+)>c(OH-) | |
| B. | 将等体积、等物质的量浓度的NH4HCO3与NaCl溶液混合,析出部分NaHCO3晶体后的溶液:c(H+)+c(H2CO3)=c(OH-)+c(CO32-)+c(NH3•H2O) | |
| C. | 向饱和氯水中加入NaOH溶液至pH=7,所得溶液中:c(Na+)>c(ClO-)>c(Cl-)>c(OH-) | |
| D. | 向0.10mol•L-1 Na2CO3溶液中通入少量CO2的溶液中:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3) |
16.现有一种铝和镁的混合物样品.某学生分别取0.9g此样品进行四次反应,并收集标准状况的氢气.有关数据记录如下表:
(1)请写出固体与NaOH溶液反应的化学方程式2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
(2)请计算固体中铝、镁的物质的量.
| 实验序号 | 固体质量 | 加入某浓度盐酸的体积/mL | 加入某浓度NaOH的体积/mL | 收集到气体体积/mL |
| 1 | 0.9 | 20.0 | ─ | 1008 |
| 2 | 0.9 | 30.0 | ─ | 1008 |
| 3 | 0.9 | ─ | 20.0 | 672 |
| 4 | 0.9 | ─ | 30.0 | 672 |
(2)请计算固体中铝、镁的物质的量.
13.在标准状况下进行下列实验,各取30.0mL同浓度的盐酸,加入同一种镁铝合金的粉末产生气体,有关数据如表所示:
下列说法正确的是( )
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量(mg) | 255 | 385 | 459 |
| 标准状况下气体的体积(mL) | 280 | 336 | 336 |
| A. | 甲、乙组的实验中,盐酸均是过量的 | B. | 盐酸的物质的量浓度为0.8mol L-1 | ||
| C. | 合金中镁、铝的物质的量之比为1:1 | D. | 丙组中铝的物质的量为0.0045mol |
14.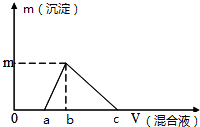 往100mL0.1mol/L NaOH溶液中逐滴滴入浓度均为0.1mol/L的氯化铝和盐酸的混合溶液,测得生成沉淀的质量(g)与滴入的混合液的体积(mL)的关系如图所示,则下列说法正确的是( )
往100mL0.1mol/L NaOH溶液中逐滴滴入浓度均为0.1mol/L的氯化铝和盐酸的混合溶液,测得生成沉淀的质量(g)与滴入的混合液的体积(mL)的关系如图所示,则下列说法正确的是( )
 往100mL0.1mol/L NaOH溶液中逐滴滴入浓度均为0.1mol/L的氯化铝和盐酸的混合溶液,测得生成沉淀的质量(g)与滴入的混合液的体积(mL)的关系如图所示,则下列说法正确的是( )
往100mL0.1mol/L NaOH溶液中逐滴滴入浓度均为0.1mol/L的氯化铝和盐酸的混合溶液,测得生成沉淀的质量(g)与滴入的混合液的体积(mL)的关系如图所示,则下列说法正确的是( )| A. | a=25mL | B. | b=33mL | C. | c=100mL | D. | m=0.195g |