题目内容
4.用锌块与30mL3mol/L盐酸反应制取H2气体,若要增大反应速率,可采取的措施是( )①再加入30mL3mol/L盐酸
②改用30mL6mol/L盐酸
③改用粉末状锌
④适当升高温度
⑤加入几滴CuSO4溶液.
| A. | ①②④ | B. | ②③④ | C. | ①③④⑤ | D. | ②③④⑤ |
分析 若要增大反应速率,可通过增大氢离子浓度、适当升高温度、增大锌表面积、构成原电池等都可以实现,以此来解答.
解答 解:①再加入30mL3mol/L盐酸,氢离子浓度不变,反应速率不变;
②改用30mL6mol/L盐酸,氢离子浓度增大,反应速率加快;
③改用粉末状锌,增大接触面积,反应速率加快;
④适当升高温度,反应速率加快;
⑤加入几滴CuSO4溶液,构成原电池,反应速率加快,
故选D.
点评 本题考查化学反应速率的影响因素,为高频考点,把握常见的影响速率的因素为解答的关键,侧重分析与应用能力的考查,注重迁移应用能力的训练,题目难度不大.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
14.在一定温度下,下列叙述是可逆反应A(g)+3B(g)?2C(g)达到平衡的标志的是( )
| A. | 正反应速率与逆反应速率相等且为零 | |
| B. | A、B、C的浓度不再变化 | |
| C. | A、B、C的物质的量相等 | |
| D. | A、B、C的分子数目比为1:3:2 |
12.下面是某化学兴趣小组的同学学习元素周期律时设计的两套实验方案.
【实验一】实验步骤如下:
(1)设计该实验方案的目的是:探究同周期元素的性质(或金属性与非金属性)的递变规律.
(2)实验①的现象是生成浅黄色沉淀,反应的化学方程式是Cl2+Na2S=S↓+2NaCl.
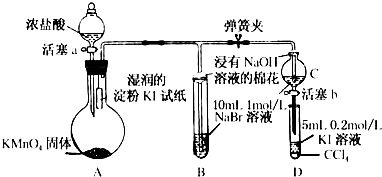
【实验二】为验证Cl2、Br2的非金属性强弱,设计了如下实验:(可供选择的试剂有:氯水、溴水、NaCl溶液、NaBr溶液、酒精、四氯化碳)实验步骤如图.
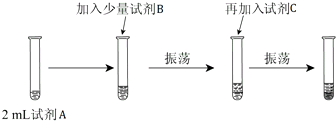
(3)试剂A是NaBr溶液;试剂B是氯水;试剂C是四氯化碳.
(4)试剂C在实验中所起的作用是萃取生成的溴,使现象更明显,
加入C振荡、静置后看到的现象是:液体分成两层,上层接近无色、下层为橙色.
以上反应可以证明Cl2的非金属性强于(填“强于”或“弱于”)Br2的非金属性,反应的离子方程式为:Cl2+2Br-=2Cl-+Br2.
【实验一】实验步骤如下:
| 实验序号 | 实验步骤 |
| ① | 向新制的Na2S溶液中滴加新制的氯水 |
| ② | 将镁条投入1mol/L的稀盐酸中 |
| ③ | 将铝条投入1mol/L的稀盐酸中 |
(2)实验①的现象是生成浅黄色沉淀,反应的化学方程式是Cl2+Na2S=S↓+2NaCl.
【实验二】为验证Cl2、Br2的非金属性强弱,设计了如下实验:(可供选择的试剂有:氯水、溴水、NaCl溶液、NaBr溶液、酒精、四氯化碳)实验步骤如图.

(3)试剂A是NaBr溶液;试剂B是氯水;试剂C是四氯化碳.
(4)试剂C在实验中所起的作用是萃取生成的溴,使现象更明显,
加入C振荡、静置后看到的现象是:液体分成两层,上层接近无色、下层为橙色.
以上反应可以证明Cl2的非金属性强于(填“强于”或“弱于”)Br2的非金属性,反应的离子方程式为:Cl2+2Br-=2Cl-+Br2.
16.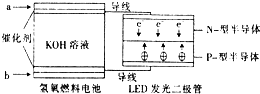 LED产品的使用为城市增添色彩.图是氢氧燃料电池驱动LED发光的一种装置示意图.下列有关叙述正确的是( )
LED产品的使用为城市增添色彩.图是氢氧燃料电池驱动LED发光的一种装置示意图.下列有关叙述正确的是( )
 LED产品的使用为城市增添色彩.图是氢氧燃料电池驱动LED发光的一种装置示意图.下列有关叙述正确的是( )
LED产品的使用为城市增添色彩.图是氢氧燃料电池驱动LED发光的一种装置示意图.下列有关叙述正确的是( )| A. | P-型半导体连接的是电池负极 | |
| B. | b处为电池正极,发生了还原反应 | |
| C. | a处通入氢气,发生还原反应 | |
| D. | 该装置中只涉及两种形式的能量转化 |
13.下列关于浓HNO3与浓H2SO4的叙述正确的是( )
| A. | 常温下都不可用铝制容器贮存 | |
| B. | 常温下都能与铜较快反应 | |
| C. | 露置于空气中,溶液浓度均降低 | |
| D. | 在空气中长期露置,溶液质量均减轻 |
14.下列各组化合物中,化学键的类型相同的是( )
| A. | CaCl2和Na2S | B. | Na2O和H2O | C. | CO2和NaCl | D. | HCl和NaOH |
 ?
?